A Tabela Periódica é composta por 118 elementos químicos. Um dos exemplos é o elemento radioativo estrôncio, classificado como metal alcalino-terroso, do grupo 2A da tabela. De forma geral, possui número atômico 38, ou seja, 38 prótons e 39 elétrons. Além disso, a massa atômica é 87,6 u.
Por possuir características radioativas, o elemento químico em questão é prejudicial à saúde. Isso porque, o raio atômico que emite é semelhante a outro elemento, o cálcio. Sendo assim, o organismo absorve o estrôncio como se fosse cálcio e as partículas radioativas se alojam no tecido ósseo.
Uma das consequências das partículas radioativas no organismo, a longo prazo, é o surgimento de células cancerígenas no tecido ósseo. Apesar de não apresentar funções no organismo humano, o estrôncio faz parte da funcionalidade de outros seres vivos, como corais rochosos. Além do mais, o elemento pode ser encontrado em exoesqueletos de criaturas abissais – seres aquáticos que vivem em zonas profundas dos oceanos.
Características do estrôncio
Em síntese, o estrôncio é um elemento químico da família dos metais alcalino-terrosos e possui símbolo Sr. Assim como os demais metais, em contato com oxigênio, ocorre a rápida oxidação e mudança na tonalidade do elemento. Ou seja, em condição ambiente, o estrôncio possui coloração prateada brilhante. Quando em contato com o oxigênio, por exemplo, o composto químico adquire cor amarelada.
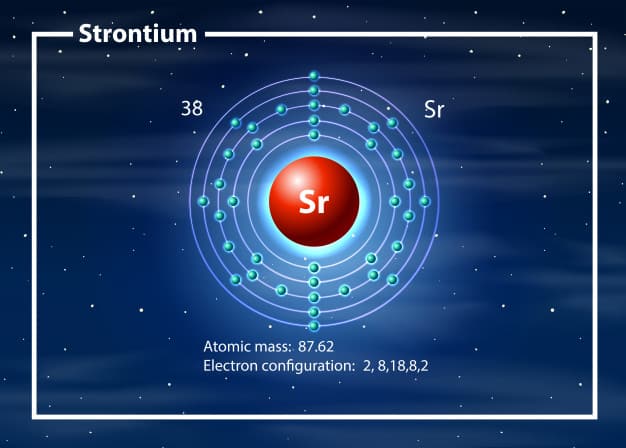
Para que não ocorra oxidação, o composto deve ser conservado imerso em querosene. Além disso, o elemento é considerado um composto químico por conta da combinação com outros elementos. Em contato com a água, o composto libera partículas de hidrogênio que formam hidróxidos.
Na natureza, o elemento químico é encontrado na forma de sulfatos e carbonatos. Dessa forma, quando em temperatura ambiente, é encontrado no estado sólido, sendo mais abundante em minerais como a estroncianite (SrCO3) e a celestite (SrSO4). Ambos os minerais são mais comuns nos EUA, na Alemanha, Reino Unido e no México, encontrados em abundância na crosta terrestre.
Descoberta do estrôncio
O estrôncio foi descoberto, em 1787, pelo químico irlandês Adair Crawford. Na época, o químico chamava o elemento de “desconhecida terra”, por conta da coloração e do aspecto prateado e mole. Mais tarde, em 1791, Thomas Charles Hope começou a estudar as anotações de Crawford de forma mais aprofundada.
Nesse sentido, Hope chegou à conclusão que a “desconhecida terra” era, na verdade, um novo elemento químico. Além disso, percebeu que o estrôncio produzia um efeito diferente e curioso. Ou seja, o efeito era a mudança de cor quando em contato com altas temperaturas, como posto em uma fogueira, por exemplo.

Já em 1809, mais ou menos, na cidade de Londres, o químico britânico Sir Humphry Davy conseguiu isolar quantidades pequenas do elemento no estado metálico. O procedimento foi possível por meio da eletrólise, utilizada, também, para produzir outros elementos, como o potássio e o sódio. A partir disso, foi declarada de forma oficial a existência de um novo elemento, o estrôncio.
Aplicações do elemento químico
O estrôncio é caracterizado como um metal mole que possui aspecto prateado, sendo sólido em temperatura ambiente. Quando em contato com altas temperaturas e oxigênio, o metal produz uma chama carmesim, mais parecida com um vermelho bem forte. Por conta disso, indústrias de pirotecnia utilizam o composto para formar fogos de artifício.
Outra utilização do elemento químico é por fábricas de tintas, que usam compostos à base de estrôncio e alumínio para produzir tintas que brilham no escuro. Indústrias do setor de higiene bucal também utilizam sais de estrôncio em creme dental. Os sais servem para diminuir a sensibilidades dos dentes, por meio do cloreto de estrôncio hexa-hidratado (SrCl2.6H2O) .

Já na mineração, o elemento químico é bastante utilizado na produção de ímãs de terras raras. Além disso, em tubos de raios catódicos contidos em televisores coloridos o elemento é utilizado para filtrar os raios X. Dessa forma, a filtragem evita que os raios X atinjam os telespectadores.
O elemento químico também pode ser utilizado para:
- Refinamento do metal zinco, por meio do processo de eletrólise;
- Produção de ímãs de ferrite;
- Dessulfurizar o aço e produzir ligas metálicas;
- Em alguns casos, o estrôncio é utilizado como pedra preciosa;
- O isótopo radioativo do estrôncio – Sr-89, é utilizado em tratamentos contra câncer. Já o Sr-85 é usado na radiologia e, por fim, o Sr-90 possui utilização em geradores que funcionam por meio de energia autônoma.
O que achou da matéria? Se gostou, leia também o que são Correntes de Convecção e e quais as características do Bário.
Fontes: Info Escola, Mundo Educação, Quimlab e Tabela Periódica
Imagens: Stuff, Freepik, Características e Astrométrico