As reações químicas são modificações da matéria de substâncias reagentes que formam os produtos. Também são denominadas de fenômenos químicos. Para que isso ocorra, no entanto, é preciso algumas condições especiais. Os reagentes têm que entrar em contato, ter afinidade química entre eles, além de colisão real entre suas moléculas e a energia de ativação.
O balanceamento das reações será alcançado quando a soma das massas dos reagentes corresponderem à das massas dos produtos. É a aplicação da Lei de Lavoisier, qual seja: “na natureza nada se cria e nada se perde, tudo se transforma.”
Há quatro tipos de reações: de síntese ou adição, de análise ou decomposição, de deslocamento e de dupla-troca. E elas estão presentes em nosso cotidiano, como na maçã que escurece ao ser partida.
O que são reações químicas?
Reações químicas (ou fenômenos químicos) podem ser conceituadas como aquilo que resulta das substâncias que são transformadas. Nelas os átomos modificam seu estado original, posto que se colocam em um novo arranjo. É assim que os compostos químicos se alteram e produzem moléculas novas, só que sem alterar os átomos dos elementos. Importante frisar que o estudo das reações químicas é uma matéria essencial, posto que está na base da Química.

Nas reações químicas existem dois tipos de substâncias principais, a saber: reagentes e produtos. Os primeiros são aqueles componentes originais que, após misturados, ocasionam uma reação entre eles. Já os produtos são aquilo que resulta da reação. Na fórmula geral temos:
REAGENTES → PRODUTOS
Nem toda mistura de reagentes, no entanto, resultará em uma reação, posto que se exigem certas condições para isso.
Condições para que Ocorram as Reações Químicas
A ocorrência das reações químicas ficam vinculada a determinadas condições. É necessário que haja contato entre os reagentes, afinidade química entre eles, além de colisão real entre suas moléculas e a energia de ativação.
Contato entre os Reagentes
Entrar em contato é uma condição necessária para que as moléculas dos reagentes colidam entre si. Um bom exemplo é usar o elemento metálico sódio para reagir com a água e produzir o hidróxido de sódio. O sódio produz a alcalinização do meio onde ocorre a reação, sem contar que o hidrogênio é produzido na reação. E assim ocorre a queima do hidrogênio com o oxigênio do ar, ajudada pelo calor que sai da reação. Todo esse complexo processo é representado pela fórmula:
Na(s) + H2O(l) → NaOH(aq) + H2(g)
H2(g) + O2(g) → H2O(l)
Afinidade Química
Já a afinidade química é a aptidão que uma substância possui de reagir com a outra. E isso é interessante porque, ainda que se coloque certas substâncias em contato, faltando afinidade inexistirá reação. No exemplo do sódio, se ele fosse deixado em contado com a querosene, jamais reagiriam, já que falta afinidade química.
Colisão Real
Para saber da colisão real entre as moléculas e a energia de ativação, vamos nos socorrer na Teoria das Colisões. Segundo ela, é preciso que as moléculas dos reagentes colidam de forma satisfatória para o sucesso da reação química. E a velocidade com que tais reações ocorrerão fica vinculado ao número de colisões favoráveis. Quanto mais colisões, mais rápida a reação.
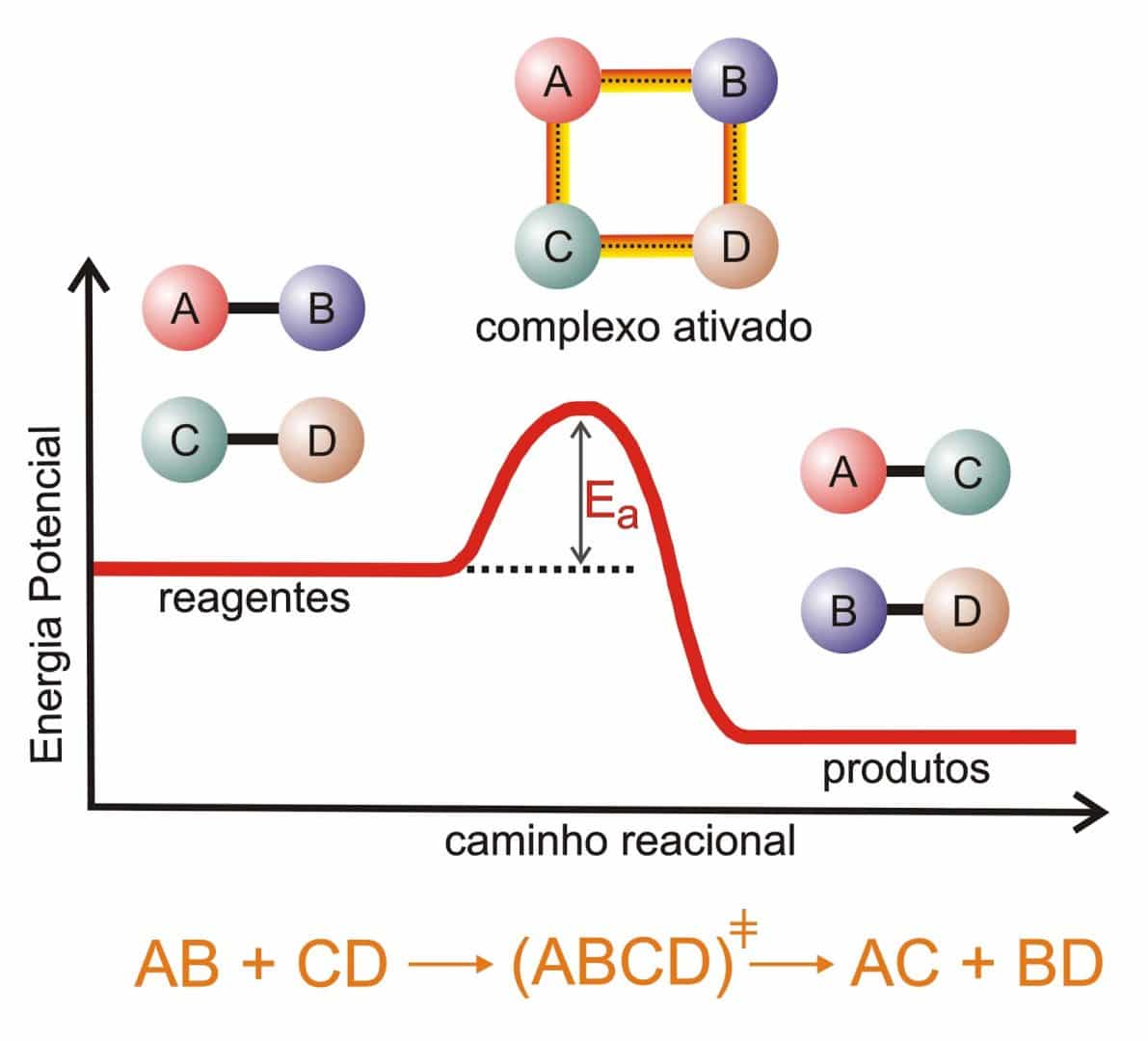
De qualquer forma, é preciso que haja um mínimo de energia nos reagentes, senão as reações químicas não se efetivarão. É a chamada energia de ativação (Eat), porquanto condição essencial para a formação do complexo ativado. Trata-se aqui de uma estrutura que está no meio entre reagentes e produtos. As ligações dos reagentes vão perdendo força, enquanto a dos produtos se formam.
Balanceamento e Cálculo da Velocidade das Reações Químicas
O químico francês Antoine Laurent Lavoisier descobriu em 1785 a Lei de Conservação das Massas. Ele chegou à conclusão de que a soma total das massas dos reagentes é igual à das massas dos produtos. E então a equação química estará balanceada. Um exemplo de equação balanceada: C + O2 → CO2. Aqui vemos um carbono e dois oxigênios tanto no reagente quanto no produto.
A velocidade das reações químicas está vinculada a diversos fatores, a exemplo de temperatura, pressão e quantidade de luz. A alteração ocorre no ritmo em que o complexo ativado se desenvolve. Por isso se calcula a velocidade das reações químicas baseando na concentração tanto de reagentes, quanto de produtos. A fórmula é: Vm = variação da concentração / intervalo de tempo.
Tipos de Reações Químicas
As reações químicas são processos que causam alteração na estrutura da matéria. E na Química Inorgânica há a classificação em quatro tipos de reações. São eles: de síntese ou adição, de análise ou decomposição, de deslocamento e de dupla-troca.
De Síntese ou Adição
Na reação de síntese ou adição, duas ou mais substâncias dão origem a um só produto: A + B → C. E um bom exemplo é a reação do magnésio com o oxigênio: 2Mg(s) + 1 O2(g) → 2MgO(s). Ocorre tal reação nos foguetes sinalizadores. Na síntese ou adição, os reagentes podem ser substâncias simples ou compostas.
De Análise ou Decomposição

De Deslocamento
Na reação de simples troca ou deslocamento, uma substância simples vai reagir com uma composta. Só que dessa reação vai originar uma simples e outra composta. Na representação por fórmula: A + XY → AY + X. Vamos exemplificar colocando uma lâmina de zinco em uma solução de ácido clorídrico. O zinco então desloca o hidrogênio e forma o cloreto de zinco: Zn (s) + 2 HCl (aq) → ZnCl2(aq) + H2 (g).
De Dupla Troca
Por fim, na reação de dupla troca, dois reagentes reagirão entre si e formarão dois produtos. São duas substâncias compostas que reagem e originam outras substâncias compostas. A fórmula é: AB + XY → AY + XB. Um exemplo é quando o ácido sulfúrico e o hidróxido de bário reagem, posto que dão origem à água e ao sulfato de bário: H2SO4 (aq) + Ba(OH)2(aq) → 2 H2O(l) + BaSO4(s).
Você sabia?
Muitas reações químicas acontecem todos os dias bem próximas de nós, embora a gente nem se dê conta disso. Veja alguns exemplos:
- para que o motor do carro funcione, a gasolina é ali queimada e produz água e gás carbônico.
- a oxidação da enzima polifenol faz com que a maçã cortada fique escura após certo tempo.
- através da oxidação do ferro e consumo de oxigênio é que ocorre a ferrugem.
- as plantas realizam a fotossíntese usando luz, gás carbônico e água.
Você gostou de conhecer as reações químicas? Então vai querer ler também sobre o que é luz.
Fontes: Toda Matéria, Stoodi, Brasil Escola, Mundo Educação, Educação UOL e Mundo Educação.
Imagens: Oceano Particular, Pidid, El-Mann e Universo Curioso.