O estudo sobre os átomos passou por diversas evoluções ao longo da história. Primeiro, se pensava que um átomo era indivisível. Logo, foi comprovado que, na verdade, o átomo possuía partículas subatômicas, os elétrons, prótons e nêutrons. Assim, o átomo se torna eletricamente neutro quando há a mesma quantidade de prótons e elétrons. Porém, quando isso não ocorre, a partícula necessita dos íons para se estabilizar.
Nesse sentido, os íons são classificados pela perda ou pelo ganho de elétrons durante as ligações químicas. Ou seja, quando os elementos químicos se misturam formando uma reação, as cargas elétricas podem sofrer modificação e se desestabilizar. Dessa forma, os íons – que podem ser divididos em ânions e cátions – surgem para tornar o átomo eletricamente neutro.
Mas afinal, como identificar os íons em uma reação química? Não se preocupe, vamos descobrir!
Classificação dos íons
Os íons são compostos que perdem ou ganham elétrons durante uma reação química. Assim, quando os elétrons são perdidos, o íon é classificado como cátion, partícula com carga positiva. Alguns exemplos de cátions são: Al+3, Na+, Mg+2, Pb+4.
Agora, quando o íon ganha elétrons durante a reação e a carga se torna negativa, é classificado como ânion. São exemplos de ânions os compostos: N-3, Cl–, F-1, O-2.
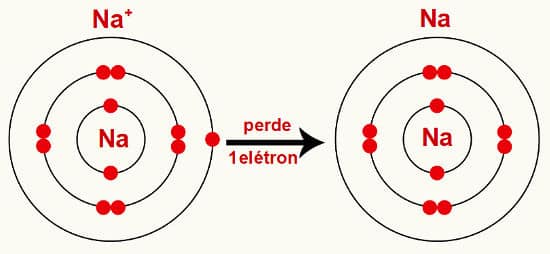
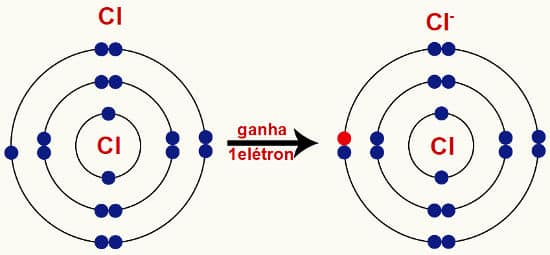
Para que compostos químicos sejam formados, como o NaCl (o sal de cozinha), ocorre a ligação entre íons positivos e negativos. Esse tipo de ligação é denominada Ligação Iônica. No caso do exemplo citado, o Cloreto de sódio, a ligação é feita da seguinte forma: Na+ + Cl– → NaCl.
Com isso, vale destacar que os ânions são partículas que possuem a quantidade de elétrons maior do que a presente nos prótons, por exemplo. Enquanto isso, os cátions possuem elétrons em menor quantidade, se comparados aos prótons.
Exemplo de reações
Para exemplificar os ânions e cátions, observe as reações à seguir:
Exemplo: 15P → 15P-3
Neste caso, é possível perceber que o átomo de fósforo (P) recebeu 3 elétrons e, dessa forma, a carga se torna negativa. Ou seja, representa um ânion.
Exemplo: 12Mg → 12Mg2+
Já neste outro exemplo, o átomo de Magnésio (Mg) perdeu elétrons. Ou seja, a reação fez o átomo se tornar um cátion com carga positiva. No caso, o elemento químico Mg2+ recebe o nome de cátion bivalente. Além disso, pode também ser chamado de íon bivalente positivo.
Potencial de Ionização e Afinidade Eletrônica
Quando falamos em potencial de ionização, estamos nos referindo à energia que um elétron necessita para sair de um núcleo atômico para outro. Essa energia depende de uma quantidade mínima, além de ser aplicada quando o composto está no estado gasoso.
Dessa forma, quando há grande quantidade de energia no elétron, ele pode se tornar, com maior facilidade, um cátion. Os halogênios, por exemplo, são compostos químicos que apresentam o potencial de ionização em maior grau, diferente dos metais.

Agora, a afinidade eletrônica se refere à capacidade do átomo de liberar espaço para a entrada de elétrons em sua atmosfera. Ou seja, se a afinidade entre um composto e outro ocorrer, os elétrons são adicionados na atmosfera do átomo por conta da grande quantidade de energia liberada. Assim, o átomo se torna um ânion.
O que achou da matéria? Se gostou, confira também o que são Elementos Radioativos e o que é Radioatividade.
Fontes: Brasil Escola, Manual da Química, Mundo Educação e Info Escola
Imagens: Beduka, Alunos Online e Química Rocheada



