Basicamente, as ligações químicas são forças de interações entre os átomos. Além disso, são responsáveis pela formação de moléculas, agrupamento de átomos ou sólidos iônicos.
Sendo assim, podem ser de três tipos: iônica, covalente e metálica. Ainda, as substâncias químicas podem ter três ligações: substâncias iônicas (ligação iônica), substâncias moleculares (ligação covalente) e substâncias metálicas (ligação metálica).
As substâncias iônicas são compostas por metal e não metal. Porém, as substâncias moleculares apresentam elementos estritamente do tipo não metal. Por outro lado, as substâncias metálicas apresentam apenas metal em sua composição.
Substâncias Iônicas
As ligações químicas que resultam em substâncias iônicas são as que ligam metal e não metal. Basicamente, são substâncias que conduzem a corrente elétrica no estado líquido, mas não no sólido.

No entanto, inclui cloreto de lítio, brometo de potássio, cloreto de cálcio, cloreto de sódio, óxido de alumínio e óxido de magnésio.
- Cloreto de lítio: LiCl, possui ponto de fusão de 80°C.
- Brometo de potássio: KBr, possui ponto de fusão de 734°C.
- Cloreto de Cálcio: CaCl2, possui ponto de fusão de 775°C.
- Cloreto de sódio: NaCl, possui ponto de fusão de 801°C.
- Óxido de alumínio: Al2O2, possui ponto de fusão de 2053°C.
- Óxido de magnésio: MgO, possui ponto de fusão de 2.825°C.
Substâncias moleculares

Basicamente, as ligações químicas que resultam em substâncias moleculares são as que fazem ligações somente do tipo não metal. No entanto, são substâncias que não conduzem corrente elétrica nem no estado líquido e nem no sólido.
Além disso, se destacam por apresentarem pontos de fusão mais baixos que as substâncias dos outros grupos. Inclui etanol, cloro, água, naftaleno, iodo e glicose.
- Etanol: C2H2O, possui ponto de fusão de -114°C.
- Cloro: Cl2, possui ponto de fusão de -102°C.
- Água: H2O possui ponto de fusão de 0 °C.
- Naftaleno: C10H8, possui ponto de fusão de 80°C
- Iodo: I2, possui ponto de fusão 114°C.
- Glicose: C6H12O6, possui ponto de fusão de 150°C.
Substâncias metálicas

A princípio, as ligações químicas que resultam em substâncias metálicas são as que apresentam somente metal em sua composição. No entanto, são substâncias que conduzem corrente elétrica tanto em estado sólido como no líquido.
Por outro lado, quanto ao ponto de fusão, essas substâncias são comparáveis ao primeiro grupo da tabela periódica. Portanto, inclui: alumínio, prata, ouro, cobre, ferro e platina.
- Alumínio: Al, possui ponto de fusão de 660°C.
- Prata: Ag, possui ponto de fusão de 962°C
- Ouro: Au, possui ponto de fusão de 1064°C.
- Cobre: Cu, possui ponto de fusão de 1085°C
- Ferro: Fe, possui ponto de fusão de 1538°C.
- Platina: Pt, possui ponto de fusão de 1768°C
Gases nobres e ligações químicas

Em síntese, todas as substâncias químicas são formadas por átomos de elementos químicos. Neste sentido, são ligações químicas entre átomos de um mesmo elemento ou entre dois, ou mais elementos.
Assim, átomos de oxigênio podem ser encontrados com outros que são iguais a ele como: O2, O3. Por outro lado, podem ser encontrados fazendo ligações químicas com outros elementos, formando diferentes substâncias.
Assim, podemos ter: CO, CO2, H2O, SO2 etc. A propósito, é importante lembrar que o oxigênio não possui existência estável isolada. Basicamente, existem milhões de substâncias com variadas ligações químicas.
Contudo, sabe-se de apenas seis, que nas quais existem átomos não unidos a outros átomos. Portanto, essas substâncias pertencem ao grupo dos gases nobres.
Neste sentido, até hoje não foi descoberta sequer uma substância natural na qual átomos de gases nobres estejam unidos a átomos de outros elementos. Os gases nobres estão presentes na atmosfera terrestre em pequena quantidade.
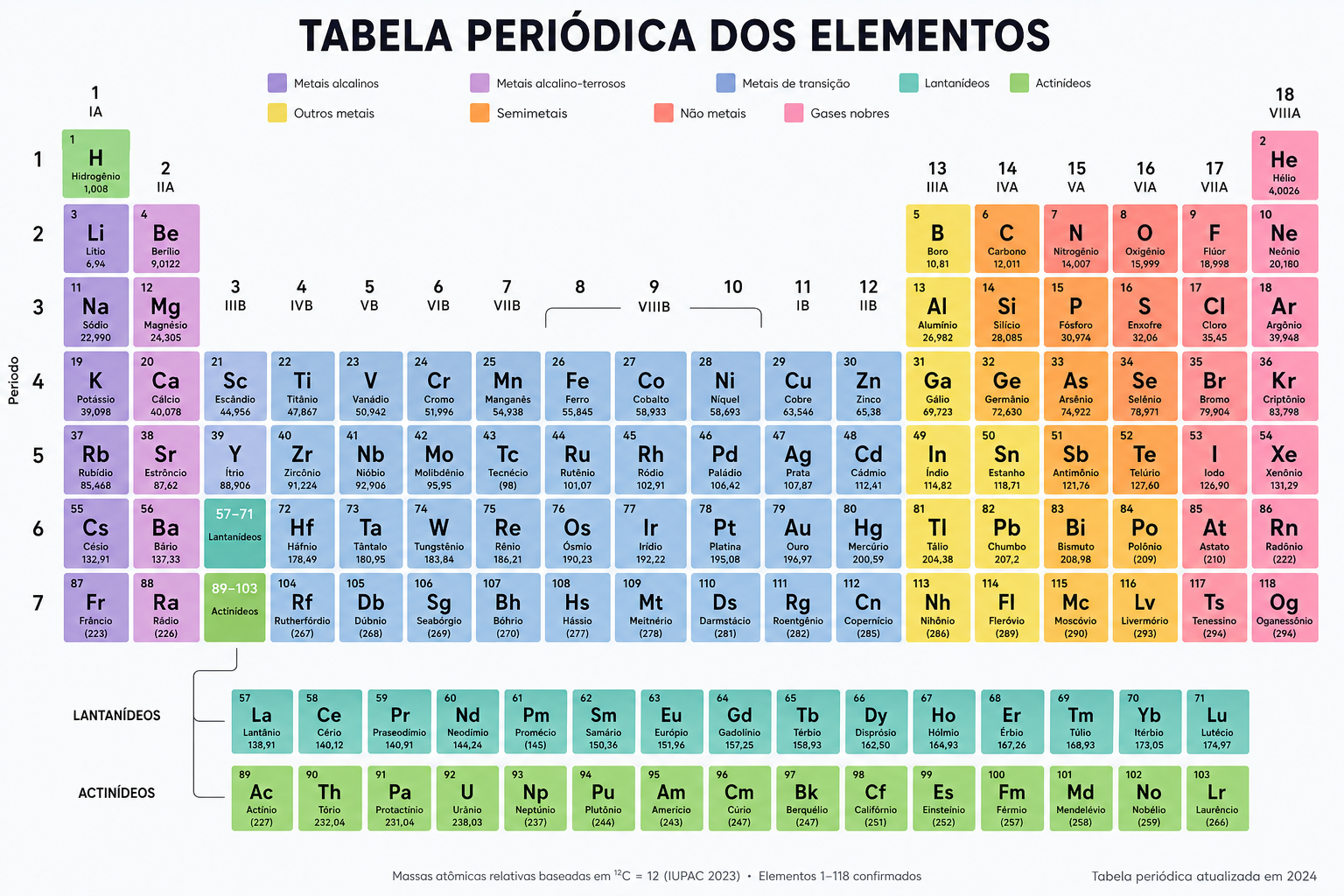
Basicamente, esses gases são formados por átomos não unidos dos elementos do grupo 18 da tabela periódica – He, Ne, Ar, Kr, Xe Rn – respectivamente, hélio, neônio, argônio, Criptônio, xenônio e radônio.
Portanto, apenas os gases nobres, nas condições ambientes apresentam átomos estáveis isolados, não unidos a outros átomos. A propósito, as observações que foram feitas a respeito dos gases nobres forneceram muitas pistas para os cientistas, no final do século XIX. Neste sentido, se esclareceu a forma que os átomos se combinam em suas ligações químicas.
Regra do octeto nas ligações químicas

A princípio, a camada de valência é a parte mais externa dos átomos com grande participação nas ligações químicas, devido ao fato do núcleo ser muito pequeno.
No entanto, como os gases nobres não formam combinações, se concluiu que a estabilidade de um átomo é compatível com a eletrosfera de um gás nobre.
Neste sentido, a regra de estabilidade de um átomo é ter 8 elétrons na última camada, com exceção do hélio que só comporta 2 elétrons na última camada.
Gás Nobre: K L M N O P
Hélio 2
Neônio 2 8
Argônio 2 8 8
Criptônio 2 8 18 8
Xenônio 2 8 18 18 8
Radônio 2 8 18 32 18 8
Portanto, seguindo essa característica dos gases nobres, Willian Kosel e Gilbert Newton Lewis, propuseram no ano de 1916 uma regra para interpretar a ligação entre os átomos, que ficou conhecida como regra do octeto de elétrons.
Ligações químicas iônicas

Basicamente, as ligações químicas do tipo iônicas são ligações em que os elementos perdem ou recebem elétrons. Para termos uma ideia sobre a perda e recebimento de elétrons, vamos considerar primeiramente os elementos do segundo período da tabela;
3Li 4Be 5B 6C 7N 😯 9F 10Ne
- N° de prótons: 3 4 5 6 7 8 9 10
- N° de camadas: 2 2 2 2 2 2 2 2
A princípio, quando observamos a configuração desses átomos, vemos que eles apresentam duas camadas com elétrons, por serem elementos do segundo período da tabela. Basicamente, os elétrons têm carga elétrica negativa e prótons, possuem carga elétrica positiva.
Neste sentido, podemos concluir que o que mantém os elétrons presos ao átomo é a atração exercida pelos prótons do núcleo, que possuem cargas positivas.
Portanto, no esquema colocado acima, vemos que no átomo do lítio, o elétron da camada de valência (camada mais externa do átomo), é atraído por 3 cargas positivas do núcleo.
Por outro lado, no berílio, os elétrons de camada de valência são atraídos por 4 cargas positivas e assim, vai aumentando o valor da carga positiva.
Basicamente, a partir desse aumento de carga positiva, podemos concluir que à medida que percorremos um período da tabela periódica da esquerda para a direita, aumenta a atração exercida pelo núcleo sobre os elétrons da camada de valência.
Elementos que perdem elétrons e recebem elétrons

Primeiramente, os átomos dos elementos dos grupos 1,2 a 13 apresentam uma tendência para perder os elétrons da camada de valência. No entanto, quando perdem os elétrons da camada de valência, a última camada eletrônica passa a ser a anterior.
Neste sentido, o átomo se estabiliza respeitando a regra do octeto. Podemos tomar como exemplo o átomo de Na, que sob determinada condição pode perder o elétron de valência.
Assim, os átomos de Mg podem perder os dois elétrons de valência e os átomos de Al podem perder os três. A princípio, os átomos dos elementos dos grupos 15, 16 e 17 apresentam tendência para receber elétrons para se estabilizar com oito elétrons na última camada.
Neste sentido, podemos pegar como exemplo átomos de F e Cl que sob determinadas condições podem receber um elétron. Por outro lado, átomos de O e S podem receber dois e átomos de N ou P podem receber três.
Portanto, baseado nas tendências dos elementos químicos de perder e receber elétrons se chegou a uma regra mais generalista: metais têm tendência a formar cátions por perder elétrons e não metais, a formar ânions por receber elétrons.
Neste sentido, os elementos do grupo 1,2 e 13 que são metais, apresentam 1,2 e 3 elétrons respectivamente na camada de valência. No entanto, para ficarem estáveis, seguindo a regra do octeto, deverão perder esses elétrons.
Por outro lado, os elementos dos grupos 15, 16 e 17, que são não metais, deverão receber o número de elétrons que faltam para completar o octeto.
Então, gostou da matéria? Se gostou, leia também: Carbono o que é? Características, onde é encontrado e ligações
Fontes: Brasil Escola, Toda Matéria, Blog Biologia Total, Unifebe
Bibliografia:
ARAúJO, Laysa Bernardes Marques de. “Ligações químicas”; Brasil Escola. Disponível em: https://brasilescola.uol.com.br/quimica/ligacoes-quimicas.htm. Acesso em 02 de julho de 2021.
BATISTA, Carolina, Ligações químicas, Toda Matéria. em https://www.todamateria.com.br/ligacoes-quimicas/
JUBILUT, Paulo. Ligação química: tipos, conceito e definição – Biologia Total, em
, https://blog.biologiatotal.com.br/ligacoes-quimicas-tipos-conceito-e-definicao/,
SCHMITT, Joelson. Ligações químicas, o que são q quia ses tipos, Unifebe, 2018, em https://www.unifebe.edu.br/site/blog/ligacoes-quimicas-o-que-sao-e-quais-seus-tipos/