Os tipos de misturas são porções de matéria que correspondem à reunião de duas ou mais substancias puras. Neste sentido, para compreendermos essas misturas e toda sua conceituação é necessário compreender primeiro a definição de substância pura.
Portanto, a substância pura é um composto molecular que não está misturada com outras substâncias. Desta forma, ela possui características singulares. No entanto, essas características são vistas como propriedades.
Assim, toda substância tem propriedades definidas que a tornam diferentes entre si. Dentre essas propriedades estão: o ponto de fusão, ponto de ebulição, densidade, o fato de ser inflamável ou não, a cor, o odor etc.
Tipos de misturas

A princípio, as misturas, na sua grande maioria, não apresentam pontos de fusão e pontos de ebulição definidos. Neste sentido, todos os tipos de misturas se diferenciam das substâncias puras, as quais apresentam pontos de fusão e ebulição constantes.
Por outro lado, constituem exceção algumas misturas de sólidos:
- Eutéticas: misturas sólidas que se fundem à temperatura constante. A propósito, a solda utilizada na eletrônica é uma mistura eutética com 37% de chumbo e 63% de estanho.
- Azeotrópicas: Algumas misturas de líquidos que fervem à temperatura constante. Neste caso, o álcool e a água formam misturas azeotrópicas com 96% de álcool e 4% de água.
Misturas heterogêneas e misturas homogêneas

Basicamente, os tipos de misturas heterogêneas não possuem as mesmas propriedades em toda a sua extensão. Neste sentido, uma mistura de ferro e enxofre em pó resulta em uma mistura sem propriedades iguais em todos os seus pontos. Assim, as características do ferro e as do enxofre são bem diferentes, veja:
- Ferro: Cor cinza-metálica, ponto de fusão = 1.538°C etc.
- Enxofre: Cor amarela, ponto de fusão = 115°C etc.
Por outro lado, uma mistura homogênea ou solução tem as mesmas propriedades em todos os seus pontos. Neste sentido, se colocarmos uma pitada de açúcar numa porção de água pura e mexermos, se obterá uma mistura com as mesmas propriedades em toda sua extensão.
Assim, se provarmos uma gota dessa solução, e depois tomarmos uma porção maior, veremos que ela tem o mesmo gosto em qualquer quantidade. Além disso, quaisquer porções dessa mistura apresentam a aparência incolor e tem a mesma densidade, compartilhando as mesmas propriedades.
Alguns tipos de misturas e suas terminações

- Enxofre e ferro: a mistura de pó de ferro e pó de enxofre é heterogênea
- Água e açúcar: mistura homogênea
- Água e óleo: mistura heterogênea.
A princípio, quando alguma substância é misturada à água e resulta em uma mistura homogênea dizemos que a substância foi dissolvida na água e foi obtida uma solução aquosa.
Neste sentido, a água que atua dissolvendo a substância é denominada solvente e a substância que foi dissolvida tem o nome de soluto. Assim, quando misturamos água e sal, a água é solvente e o sal é o soluto.
Por outro lado, quando dois líquidos formam uma mistura homogênea, dizemos que eles são miscíveis. Desta forma, água e álcool comum (etanol ou álcool etílico) são líquidos miscíveis.
Porém, quando dois líquidos formam misturas heterogêneas são denominados líquidos imiscíveis. Assim, temos como exemplo o óleo e a água.
Fases de uma mistura

A princípio, o conceito de fase é muito utilizado para o estudo de qualquer amostra de matéria, seja ela substância pura ou relacionada aos tipos de misturas.
No entanto, a definição de fase se relaciona a uma porção de uma amostra de matéria que apresenta as mesmas propriedades e todos os seus pontos. Porém, uma fase pode se apresentar contínua ou fragmentada em várias partes.
Contudo, para termos uma ideia mais concreta sobre as fases de uma mistura, vamos imaginar algumas misturas. Portanto, vamos considerar uma mistura de óleo e água. A partir desse exemplo veremos que essa mistura é uma mistura heterogênea de duas fases contínuas, pois uma fase é água e a outra fase é óleo.
Por outro lado, se considerarmos uma mistura de ferro e enxofre veremos que os pequenos grãos de ferro constituem uma fase, e os pequenos grãos de enxofre constituem a outra fase.
Neste sentido, essa mistura mostra-se diferente da mistura de água e óleo, por se caracterizar de forma fragmentada em muitas partes – grãos de ferro e grãos de enxofre. Contudo, em uma mistura de água e açúcar, que é homogênea, existe só uma fase.
Assim, esta característica pode ser estendida para todas as misturas homogêneas. Diante de todas essas experiências concretas, se estabelece a seguinte regra: uma mistura homogênea apresenta uma só fase e uma mistura heterogênea apresenta duas fases ou mais.
Curva de aquecimento em substâncias e misturas

Quando comparamos a curva de aquecimento de uma substância pura, vemos que esta obedece a algumas constâncias, onde as transformações da matéria sempre ocorrem nas mesmas temperaturas.
Neste sentido, a água possui o seu ponto de fusão de 0°C e seu ponto ebulição de 100°C. Quando submetemos a água em uma curva que inicia em -20°C e posteriormente se acrescenta um aquecimento contínuo. Assim, veremos a realização de uma curva constante: sólido de -20°C até 0°C – líquido de 0°C até 100°C – e a partir de 100°C, vapor.
Por outro lado, quando se repete o mesmo experimento com água e cloreto de sódio, vemos que a mistura quando colocada no congelador, não congela a 0°C, e sim abaixo dessa marca dependendo da quantidade de sal acrescentado à água.
No entanto, outra característica que varia em relação à substância pura, é que a temperatura não permanece constante durante o congelamento, mas diminui gradualmente.
Além do mais, quando se aquece essa mistura, iremos perceber que ela não entra em ebulição a 100°C e assim começa a ferver acima de 100°C (dependendo da quantidade de sal acrescentado) e a temperatura não permanece constante durante a ebulição, aumentando gradualmente.
Obtenção de substâncias puras a partir de misturas
A princípio, as misturas podem ser separadas e para obter substâncias puras, os principais métodos de separação de misturas heterogêneas, são:
- Decantação: mais utilizada para separar tipos de misturas heterogêneas formadas por duas fases como, por exemplo, água e área. Neste sentido espera-se a areia mais densa que a água se deposite no fundo do recipiente (sedimentação). Posteriormente pode-se transferir a água para outro recipiente inclinando-se lentamente o frasco da mistura, essa técnica é denominada decantação.
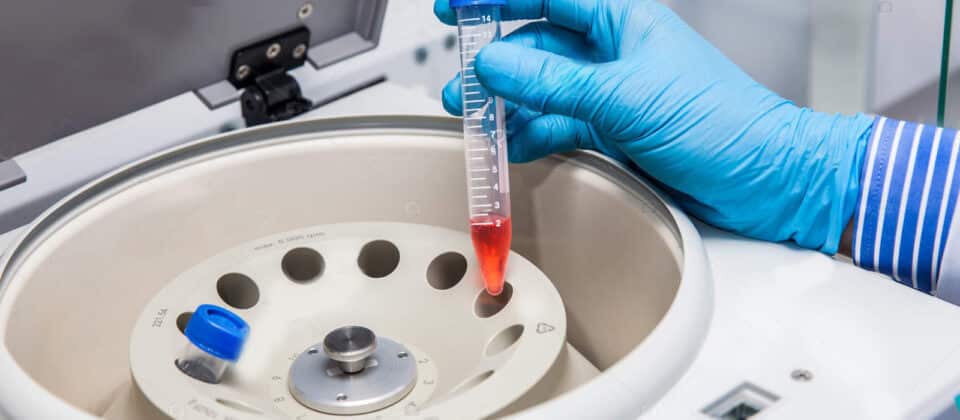
- Centrifugação: No caso da decantação ser muito lenta, podemos utilizar a centrifugação, intensa rotação realizada em centrífugas.
Filtração simples e a vácuo:
A filtração simples consiste em despejar a mistura sobre uma superfície porosa apropriada (filtro de papel ou outros materiais). A propósito, o processo do filtro é muito semelhante ao da peneira.
Por outro lado, na filtração a vácuo, o papel filtro é ajustado à superfície de um funil apropriado (funil de Buchner), que é conectado à boca de um frasco especial, o Kitassato.
Além disso, o dispositivo denominado trompa d’água (a trompa de vácuo) é ligado ao Kitassato. Dessa forma, dentro da trompa passa água corrente que arrasta o ar consigo.
Assim, esse processo remove um pouco de ar de dentro do kitassato e faz a pressão interna ficar menor que a atmosférica. Neste sentido, a pressão atmosférica força a fase líquida da mistura a passar mais rápido pelo papel de filtro.
Tipos de misturas e outras técnicas de separação

- Funil de separação
- Dissolução fracionada
- Ventilação
- Levigação
- Peneiração
- Flotação
- Sifonação
- Evaporação
- Destilação simples
- Destilação racionada
Gostou da matéria? Se gostou, leia também: Lei de Dalton o que é? Definição, teoria e mistura gasosa
Fontes: Manual de Química, Brasil Escola, Mundo Educação, Prepara Enem
Imagens: Pexels, Blog Labor, Flickr
Bibliografia
DIAS, Diogo L. Tipod de Mistura, Manual de Química, disponível em, https://www.manualdaquimica.com/quimica-geral/tipos-misturas.htm,
FERREIRA. Victor, R. Misturas: Conceitos, tipos, métodos de separação, Mundo Educação, em https://mundoeducacao.uol.com.br/quimica/tipos-misturas.htm,
FOGAÇA, Jennifer Rocha Vargas. “Tipos de Misturas”; Brasil Escola. Disponível em: https://brasilescola.uol.com.br/quimica/tipos-misturas.htm. Acesso em 07 de julho de 2021.
FOGAÇA, Jennifer Rocha Vargas. Tipos de Misturas, Brasil Escola. Disponível em: https://www.preparaenem.com/quimica/tipos-misturas.htm



