A polaridade das moléculas faz relação à distribuição dos elétrons ao redor de seus átomos. Uma distribuição feita de forma simétrica forma uma molécula apolar, enquanto uma distribuição assimétrica acaba resultando em uma molécula polar.
Todavia, podemos visualizar a polaridade das moléculas quando são submetidas a um campo elétrico externo ao ambiente em que se encontram. Nesse sentido, se uma parte das moléculas forem atraídas pelo polo positivo e outra parte atraída pelo polo negativo, pode-se dizer que temos uma molécula polar.
Entretanto, quando as moléculas não se orientam, ou seja, não se sentem atraídas por nenhum dos polos, estamos diante de uma molécula apolar. Para análise da polaridade das moléculas, utiliza-se dois critérios: diferença de eletronegatividade entre os átomos e a geometria molecular.
Polaridade das moléculas: eletronegatividade dos átomos
Para determinar a polaridade das moléculas, um dos critérios usados é a eletronegatividade dos átomos. Por eletronegatividade, entende-se como a capacidade de um átomo em atrair elétrons que foram compartilhados com outro átomo, em uma ligação covalente.

Todavia, se dispomos de moléculas formadas por ligações entre átomos dos mesmos elementos químicos (substâncias simples), como o oxigênio, hidrogênio, nitrogênio, cloro, fósforo, dentre outros, elas serão apolares.
No caso de uma molécula diatômica, aquela formada por dois átomos, quando possuir elementos com eletronegatividades diferentes, estamos diante de uma molécula polar. Exemplos são o ácido clorídrico e o ácido fluorídrico.
A molécula de ácido clorídrico (HCl) é polar, pois forma um polo negativo no cloro, resultado do acúmulo de carga negativa. Nesse sentido, o lado do hidrogênio acaba por receber carga positiva que se acumula e forma um polo positivo.
Geometria molecular
Outro critério usado para a determinação da polaridade das moléculas, a geometria molecular se relaciona com o modo em que os elétrons estão distribuídos em uma molécula, além da sua polaridade.
Os polos de uma molécula estão relacionados à carga parcial. Nesse sentido, a polaridade das moléculas com mais de dois átomos é determinada pelo vetor momento dipolar resultante, que leva em consideração os vetores de cada ligação polar das moléculas.
Assim, quando o resultado da soma de cada vetor é nulo, temos uma molécula apolar. Quando o resultado da soma dos vetores apresentar outro valor, estamos diante de uma molécula polar.
Nesse sentido, e usando como exemplo a molécula de CO2, observamos que o oxigênio (3,44) tem mais eletronegatividade do que o carbono (2,55), o que atrai os elétrons para o oxigênio. Assim, forma-se uma carga parcial negativa no oxigênio e o carbono apresenta carga positiva:
O ← C → O
Como os vetores desta molécula estão em sentido contrário, eles acabam por se anular. Nesse sentido, temos aqui uma molécula apolar.
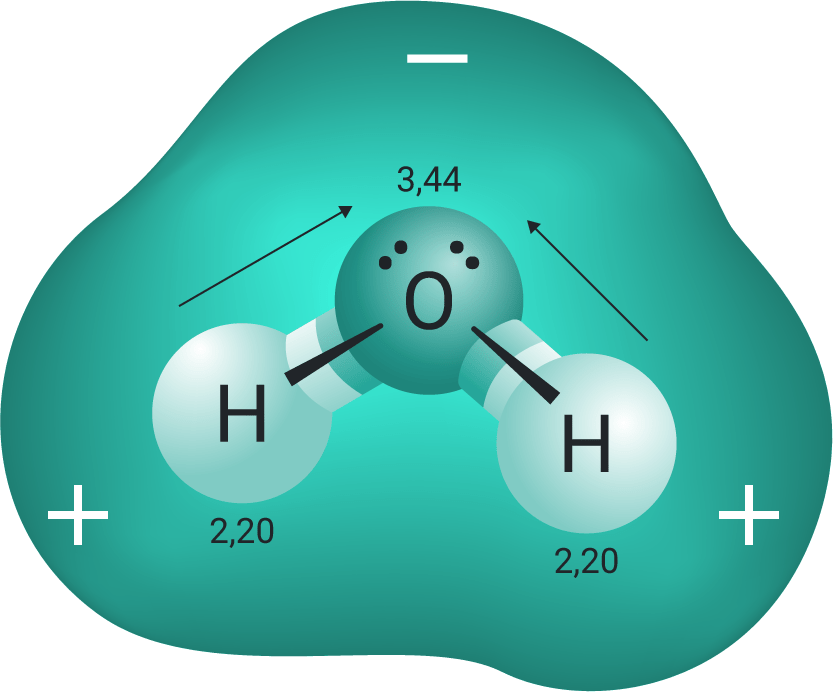
No exemplo da água (H2O), os elétrons acabam atraídos pelo oxigênio. Ainda, como os vetores não se anulam nesta molécula (vetor momento dipolar diferente de zero), pode-se afirmar que a água é polar.
Então, o que achou da matéria? Se gostou, leia também: Separação magnética, o que é? Propriedades, utilidade e vantagens.
Fontes: Brasil Escola, Manual da Química, Toda Matéria
Imagens: Blog do Enem, Vecteezy, Estácio



