Os modelos atômicos são representações teóricas que buscam descrever a estrutura e funcionamento do átomo. Então, nada mais são do que a tentativa de explicação da configuração, propriedades e comportamento de um átomo.
Esses estudos foram desenvolvidos por cientistas ao longo de muito tempo, com a principal finalidade de explicar a composição de um átomo.
Os mais conhecidos são:
- Modelo Atômico de Dalton (John Dalton, 1808)
- Modelo Atômico de Thomson (J.J. Thomson, 1897)
- Modelo Atômico de Rutherford (Ernest Rutherford, 1911)
- Modelo Atômico de Bohr (Niels Bohr, 1913)
Assim, cada modelo foi criado com base em novas descobertas e teorias que surgiram ao longo dos anos, contribuindo para a evolução da física e para o nosso entendimento da estrutura dos átomos.
Resumo dos modelos atômicos
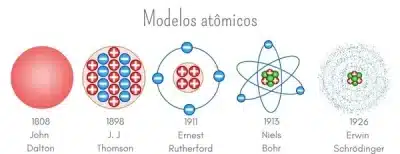
- Modelo Atômico de Dalton: Proposto em 1803, Dalton postulou que o átomo era uma esfera maciça e indivisível, e que todos os átomos de um elemento eram idênticos.
- Modelo Atômico de Thomson: Proposto em 1897, Thomson descobriu o elétron e propôs que o átomo era uma esfera carregada positivamente com elétrons dispersos dentro dela, como passas em um pudim.
- Modelo Atômico de Rutherford: Proposto em 1911, Rutherford descobriu o núcleo atômico e propôs que o átomo era constituído de um núcleo pequeno e denso carregado positivamente, com elétrons orbitando em torno dele.
- Modelo Atômico de Bohr: Proposto em 1913, Bohr propôs que os elétrons giravam em órbitas ao redor do núcleo em camadas definidas, cada uma com um nível de energia quantizada.
- Modelo Atômico de Schrödinger: Proposto em 1926, Schrödinger propôs que os elétrons eram ondas que ocupavam regiões do espaço chamadas de orbitais, com diferentes níveis de energia.
- Modelo Atômico Atual: O modelo atual da estrutura atômica é uma combinação dos modelos anteriores, que descrevem o átomo como um núcleo central positivo cercado por elétrons em órbita em camadas definidas, cada uma com um conjunto de orbitais possíveis. A estrutura atômica é descrita pela mecânica quântica e tem um comportamento ondulatório em vez de corpuscular.
Modelo atômico de Dalton

O modelo atômico de Dalton foi proposto por John Dalton em 1808. Algumas das principais características desse modelo são:
- A matéria é formada por partículas extremamente pequenas e indivisíveis chamadas átomos.
- Os átomos de um elemento químico são idênticos em massa e outras propriedades, mas diferentes dos átomos de outros elementos.
- Os átomos não são criados nem destruídos em reações químicas, apenas rearranjados.
- Os compostos químicos são formados por átomos de diferentes elementos combinados em proporções fixas e definidas.
- As reações químicas envolvem a combinação, separação ou rearranjo dos átomos.
O modelo de Dalton foi uma importante contribuição para a compreensão da estrutura da matéria e ajudou a estabelecer a teoria atômica moderna. No entanto, posteriormente foram descobertas partículas subatômicas e outras características dos átomos que não eram explicadas pelo modelo de Dalton, levando a novas teorias e modelos atômicos.
Modelo atômico de Thomson
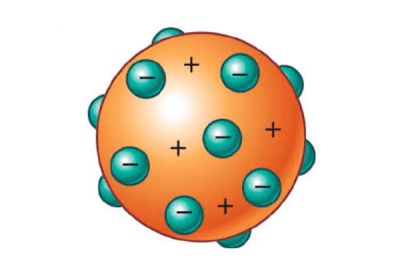
O modelo atômico de Thomson, o famoso modelo do pudim de passas, foi criado pelo físico britânico J.J. Thomson em 1897. Esse modelo foi a primeira tentativa de descrever a estrutura interna do átomo, e foi baseado em seus experimentos com raios catódicos.
Características do modelo atômico de Thomson:
- O átomo é composto por elétrons e uma esfera positiva uniforme, como um pudim de passas.
- Os elétrons estão embutidos na esfera positiva de forma aleatória.
- O número de elétrons e de cargas positivas é igual, tornando o átomo eletricamente neutro.
- O modelo não explicava a natureza das cargas positivas e como elas estavam distribuídas no átomo.
Embora o modelo de Thomson tenha sido posteriormente substituído por outros modelos mais precisos, ele foi importante por introduzir a ideia de que o átomo é composto de partículas menores e pela descoberta do elétron.
Modelo de Rutherford
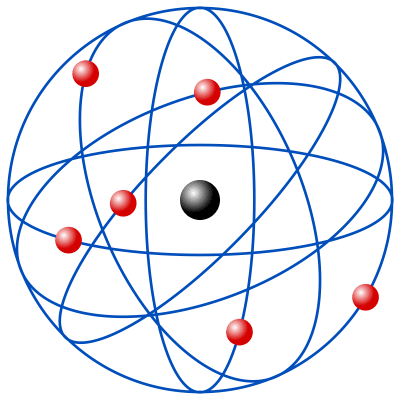
O modelo atômico de Rutherford foi proposto pelo físico neozelandês Ernest Rutherford em 1911, durante uma série de experimentos que ele e seus colaboradores realizaram para estudar a estrutura do átomo. Algumas características desse modelo incluem:
- O átomo é composto por um núcleo central, pequeno e denso, que contém a maior parte da massa do átomo e é carregado positivamente.
- Os elétrons orbitam ao redor do núcleo em órbitas circulares, como planetas em torno do sol.
- A carga elétrica total do átomo é neutra, ou seja, o número de elétrons é igual ao número de prótons no núcleo.
O modelo de Rutherford foi uma importante contribuição para a compreensão da estrutura atômica e levou à descoberta do nêutron por James Chadwick em 1932. No entanto, o modelo não explicava completamente as propriedades dos átomos, como o espectro de linhas e a distribuição de elétrons em camadas distintas. Por isso, modelos posteriores, como o modelo de Bohr e o modelo atualmente aceito, o modelo quântico-mecânico, foram desenvolvidos para expandir e aprimorar a compreensão da estrutura atômica.
Modelo atômico de Bohr
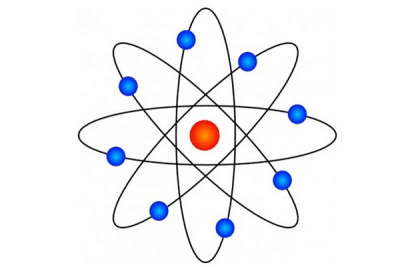
O modelo atômico de Bohr foi proposto pelo físico dinamarquês Niels Bohr em 1913, e representa um avanço importante em relação aos modelos anteriores.
As principais características do modelo de Bohr são:
- Ele propõe que os elétrons giram em torno do núcleo do átomo em órbitas circulares ou elípticas, sem emitir radiação eletromagnética. Isso é conhecido como princípio da quantização de energia, e implica que os elétrons só podem ocupar determinados níveis energéticos discretos.
- O modelo sugere que os elétrons podem saltar de uma órbita para outra, emitindo ou absorvendo um fóton de energia igual à diferença de energia entre as duas órbitas. Esse processo é conhecido como transição eletrônica, e explica a emissão e absorção de luz por átomos.
- O modelo de Bohr também introduz o conceito de número quântico, que é usado para descrever os diferentes níveis energéticos e as órbitas permitidas para os elétrons. Os números quânticos incluem o número quântico principal (n), o número quântico do momento angular (l) e o número quântico magnético (m).
- Embora o modelo de Bohr tenha sido uma importante contribuição para a compreensão da estrutura atômica, ele apresenta algumas limitações. Por exemplo, ele não leva em conta a natureza ondulatória dos elétrons, e não explica por que os elétrons não caem no núcleo devido à atração eletrostática. Essas questões foram abordadas por modelos mais avançados, como o modelo quântico-mecânico.
Modelo atômico de Schrödinger
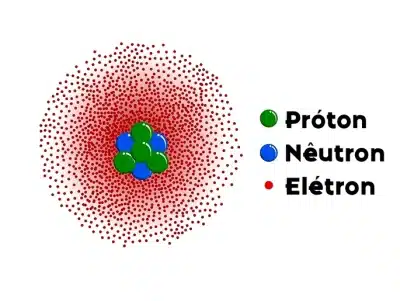
O modelo atômico de Schrödinger foi proposto pelo físico austríaco Erwin Schrödinger em 1926, como uma extensão do modelo atômico de Bohr. Algumas características desse modelo são:
- O elétron é tratado como uma onda e sua posição é descrita por uma função matemática chamada de função de onda;
- A distribuição de probabilidade da posição do elétron é descrita pela função de onda;
- A energia do elétron é quantizada, ou seja, só pode ter valores discretos;
- A função de onda é obtida através da solução da equação de Schrödinger, que leva em conta as propriedades ondulatórias do elétron e as forças que agem sobre ele.
O modelo de Schrödinger é importante porque ele permitiu entender melhor o comportamento dos elétrons nos átomos e explicar fenômenos que não podiam ser explicados pelo modelo de Bohr, como a estrutura fina das linhas espectrais. Além disso, ele abriu caminho para o desenvolvimento da mecânica quântica, que revolucionou a física do século XX.
Exercícios sobre modelos atômicos
Questão 1. (UERJ)
“O átomo é uma partícula tão pequena que não pode ser vista pelo olho humano, mas ele tem sido estudado há muitos anos.” Dentre as diferentes teorias propostas para a constituição do átomo, a mais recente foi apresentada por Niels Bohr em 1913.
Nessa teoria, o átomo é constituído por:
a) um núcleo contendo prótons e elétrons, que giram em órbitas circulares ao seu redor.
b) um núcleo contendo nêutrons e prótons, no qual se movem elétrons.
c) um núcleo contendo elétrons, nos quais se movem prótons e nêutrons.
d) uma massa distribuída de forma contínua no espaço, na qual se encontram elétrons, prótons e nêutrons.
Resposta: b) um núcleo contendo nêutrons e prótons, no qual se movem elétrons.
Questão 2. (ENEM)
Em 1897, J. J. Thomson descobriu o elétron, partícula que compõe a eletrosfera do átomo, modificando a concepção de átomo da época. Em 1913, Niels Bohr elaborou um modelo que descrevia o átomo como um sistema planetário, no qual os elétrons giravam em órbitas circulares em torno do núcleo, que era composto por prótons e nêutrons. Este modelo permitia explicar fenômenos que os modelos anteriores não conseguiam.
Nesse modelo, o átomo é eletricamente neutro, porque:
a) o número de elétrons é igual ao número de prótons.
b) o número de elétrons é igual ao número de nêutrons.
c) o número de elétrons é igual ao número de prótons e nêutrons.
d) o número de prótons é igual ao número de nêutrons.
Resposta: a) o número de elétrons é igual ao número de prótons.
Questão 3. (UFSM/RS)
O modelo atômico proposto por Bohr é considerado um modelo quântico e apresenta diversas características.
Sobre esse modelo, analise as afirmativas abaixo e assinale a alternativa correta:
I. Os elétrons descrevem órbitas circulares ao redor do núcleo.
II. A energia dos elétrons é quantizada e só podem assumir determinados valores.
III. A energia dos elétrons aumenta à medida que se afastam do núcleo.
a) Somente a afirmativa I é verdadeira.
b) Somente a afirmativa II é verdadeira.
c) Somente a afirmativa III é verdadeira.
d) As afirmativas I e II são verdadeiras.
e) As afirmativas II e III são verdadeiras.
Resposta: letra d) As afirmativas I e II são verdadeiras.
Fonte: Manual da química, Brasil Escola, Toda Matéria.


