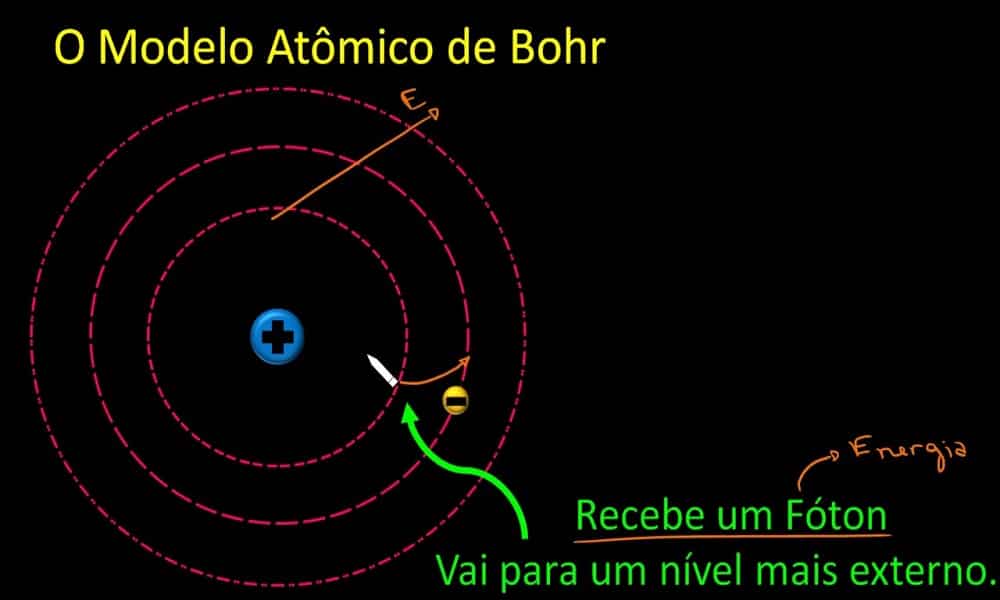
O Modelo Atômico de Bohr tem um núcleo ao redor do qual os elétrons giram em órbitas. Isso foi uma revolução, posto que bem se adequou à análise do hidrogênio.
O problema surgiu quando começou a falhar com outros elementos, levando ao seu aperfeiçoamento futuro. Esse experimento, na verdade, visou preencher as lacunas do Modelo Atômico de Rutherford.
Entre as várias conclusões de Bohr está o Princípio da Quantização da energia atômica: o elétron tem uma quantia específica de energia.
Contexto Histórico

Quando se fala em Física Nuclear, um nome se destaca: Ernest Rutherford. Ele foi o ganhador do Prêmio Nobel de Química em 1908. Destaque para seu trabalho sobre a desintegração dos elementos, assim como a química das substâncias radioativas.
E no ano de 1911 ele criou o Modelo Atômico de Rutherford, também conhecido como Modelo Planetário do Átomo. Sua teoria dizia que os átomos possuem sua carga positiva com concentração em um núcleo minúsculo.
Foi ele também que fez a primeira divisão do átomo, no ano de 1917. Orientando uma equipe, ele chegou ao experimento de dividir o núcleo de maneira controlada. Por tudo isso, Rutherford é considerado como o Pai da Física Nuclear.
A Ciência dos Átomos, no século XIX, teve destaque com os experimentos do espectro eletromagnético feitos por Robert Bünsen. Ele e seu assistente Gustav Kirchhoff estudaram os espectros provindos da emissão de vários gases. Nisso perceberam que não havia repetição no padrão das linhas espectrais, que por sua vez eram separadas por espaços vazios.
Modelo Atômico de Bohr
Quando Ernest Rutherford criou sua teoria atômica, deixou lacunas que Niels Henry David Bohr se propôs a preencher. Por essa razão, o átomo de Bohr é igualmente denominado de Modelo Atômico de Rutherford – Bohr. Eles trabalhavam juntos, o que facilitou o estudo.

O Modelo Atômico de Bohr serviu para explicar o comportamento do átomo de hidrogênio. Essa era uma das lacunas deixadas pela Teoria Atômica de Rutherford.
Ocorre que o próprio Modelo Atômico de Bohr também apresentou lacunas sem preenchimento. Isso levou seu criador a reconhecer as falhas, assim como propor um novo modelo, em 1913.
Supunha-se que os elétrons emitiam ondas eletromagnéticas, só que não se sabia como eles, ao perderem energia, não colidiam com o núcleo atômico. Hoje se sabe que o elétron, de fato, emite energia, só que, quanto maior for essa energia, mais afastado ele está do núcleo do átomo.
As Conclusões de Bohr
Na conclusão de suas pesquisas e experimentos, Bohr chegou a alguns fundamentos importantes. E um deles é o Princípio da Quantização da energia atômica, que estipula que cada elétron traz uma quantidade específica de energia.

Cada elétron tem uma órbita, ou estado estacionário, que não é fixa. É que se o elétron emite energia, ele salta para uma órbita mais afastada do núcleo. Se ele consumir energia, aumenta automaticamente o nível dessa energia. As camadas eletrônicas, ou níveis de energia, apresentam um número determinado e são denominadas pelas letras: K, L, M, N, O, P, Q.
O Modelo Atômico de Bohr igualmente concluía pela existência de órbitas onde os elétrons não ficavam, posto serem órbitas proibidas. Estas se situavam entre níveis conhecidos de energia.
O Modelo Atômico de Bohr funcionava perfeito quando analisava o hidrogênio, mas falhava quando se tratava de outro elemento. É que ele não explicava o espectro de raia, quando formado por elementos com mais número de elétrons. Foi por isso que, a partir da década de 1920, alguns cientistas melhoraram o Modelo Atômico de Bohr.
Leia também sobre a Dilatação linear – o que é, como ocorre, cálculo, coeficientes e tipos.
Fonte: Info Escola, Wikipédia, Cola da Web, Toda Matéria, Só Química, Brasil Escola, Mundo Educação, Gestão Educacional.
Fonte das imagens: Youtube, New Zealand Geographic, Youtube e Slide Share.