Uma ligação iônica ocorre quando átomos de elementos químicos doam elétrons entre si. Dessa forma, a ligação é feita para que os elementos atinjam estabilidade na camada de valência. De acordo com a Teoria do Octeto, precisam ter oito elétrons. Dessa forma, a ligação pode ocorrer em metais e ametais, e entre um metal e o hidrogênio.
O nome ligação iônica se justifica porque a ação é feita entre moléculas de cátions e ânions, ou seja, íons – átomos que perderam ou ganharam elétrons. Nesse sentido, dentro da ligação iônica, um ânion se junta a um cátion formando assim um complexo iônico. Visto isso, os ânions possuem carga elétrica negativa, enquanto os cátions são compostos por carga elétrica positiva.
Portanto, na ligação iônica os elementos que realizam ação de doar elétrons são, geralmente, aqueles formados pela família dos metais alcalinos, alcalinos-terrosos e família do boro. Por outro lado, os elementos que ganham elétrons de forma mais fácil são o nitrogênio, os calcogênios e os halogênios.
Ligação iônica e os elementos químicos
Na ligação iônica ocorre a doação de elétrons entre os átomos. Assim, é necessário entender qual a carga atômica que cada elemento químico possui. Quando um átomo recebe elétrons a carga será negativa, como nos ametais. Caso o átomo perca elétrons a carga se torna positiva, como ocorre com os metais.
Dessa forma, observe a distribuição de cargas entre os elementos químicos mais propícios para a ocorrência de ligações iônicas:
- Família dos metais alcalinos: possuem 1 elétron na camada de valência = carga +1;
- A Família dos metais alcalinoterrosos: contém 2 elétrons na camada de valência = carga +2;
- Família do boro – apresentam 3 elétrons na camada de valência = se metal, carga +3; se ametal, carga -3;
- Família do carbono – contém 4 elétrons na camada de valência = se metal, carga +3; se ametal, carga -3;
- Família do nitrogênio: apresentam 5 elétrons na camada de valência = se metal, carga +5; se ametal, carga -3;
- Família dos calcogênios: 6 elétrons na camada de valência = se metal, carga +6; se ametal, carga -2;
- Família dos halogênios: são formados por 7 elétrons na camada de valência = carga -1.
Fórmulas
Para que a fórmula de uma ligação iônica seja formada é preciso obedecer à algumas especificações. Dentre elas podemos citar a carga do cátion, ânion e o cruzamento entre as cargas. Ou seja, o valor de cada carga deve ser determinado para que a fórmula seja construída. Assim, cada elemento terá uma fórmula à partir da capacidade de perder ou ganhar elétrons.
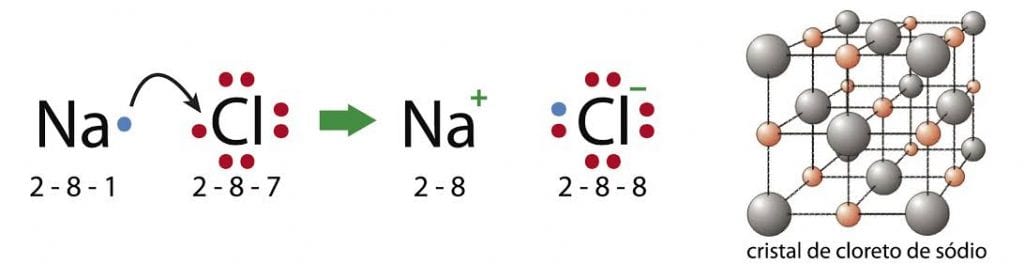
Observe os exemplos:
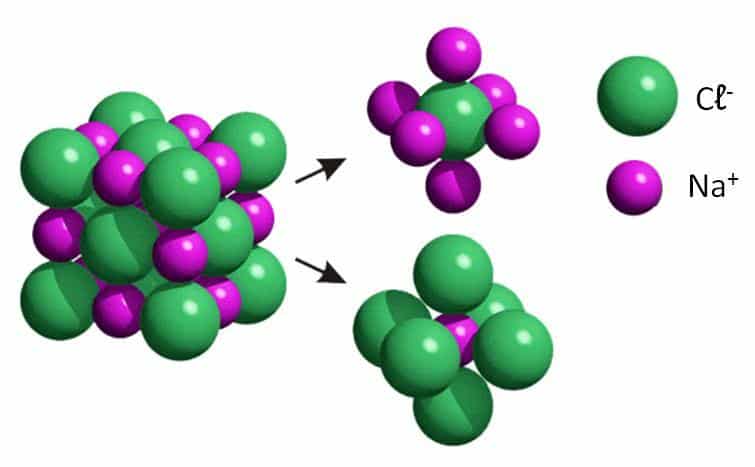
- Na+Cl– = NaCl – Cloreto de sódio, mais conhecido como o sal de cozinha;
- Mg+Cl– = MgCl2 – Cloreto de Magnésio;
- Al+O– = Al2O3 – Óxido de Alumínio.
Os elementos químicos que realizam ligação iônica apresentam algumas características específicas. Ou seja, são moléculas sólidas e os a organização dos átomos acontece para que retículos cristalinos sejam formados, além de serem solúveis na água.
Além disso, outras características compõem os elementos das ligações iônicas como a capacidade de conduzir corrente elétrica. Apresentam também nos processos de transformações químicas, elevados pontos de fusão e ebulição.
O que achou da matéria? Se gostou, já corre pra conferir mais textos aqui no site como, por exemplo, o que Efeito Estufa e Fenômenos Naturais.
Fontes: Mundo Educação, Toda Matéria e Brasil Escola
Fonte imagem destaque: Jimdo