Primeiramente, os elementos químicos são compostos por átomos, e sua estrutura ou disposição é descrita pela fórmula estrutural. Em suma, a fórmula estrutural dos elementos é um esquema que indica a estrutura dos átomos e a ligação entre eles, sendo uma das maneiras de se representar uma molécula.
A princípio, a função da fórmula estrutural é representar as ligações entre os elementos. Neste sentido, cada par de elétrons interligado entre dois átomos é simbolizado por um traço.
Desta forma, se estabelece uma ligação covalente quando os átomos se unem no compartilhamento de elétrons. Por fim, os átomos unidos por uma ligação covalente são denominados moléculas.
Tipos de fórmulas
Em síntese, na fórmula estrutural, existem três maneiras distintas de representar uma molécula: fórmula molecular, fórmula eletrônica (ou fórmula de Lewis) e a fórmula estrutural.
- Molecular: H2O (água)
Basicamente, é a representação mais simples, aponta a quantidade de átomos de elemento químico por molécula
- Eletrônica: H• •O• •H (água).
A princípio, conhecida como fórmula de Lewis, indica os elétrons da camada de valência de cada átomo e a formação dos pares eletrônicos. Além disso, também aponta os elementos e o número de átomos envolvido.
- Estrutural: H – O – H (água)
Contudo, de forma diferente das outras duas, esta fórmula indica a ligação entre os elementos, na qual um traço representa o par de elétron compartilhado entre os átomos.
Fórmula estrutural plana
A fórmula estrutural plana mostra os elementos e os números de átomos envolvidos na ligação. A princípio, na fórmula plana, são utilizados traços para representar as ligações entre os elementos, são três tipos de ligações:
- Simples: compartilhamento de dois elétrons entre os átomos:
- Dupla: compartilhamento de 4 elétrons entre os átomos:
- Tripla: compartilhamento de 6 elétrons entre os átomos
Fórmula estrutural condensada
Na fórmula estrutural condensada ou simplificada acontece uma abreviação do esquema com a utilização de números para quantificar os átomos.
Neste sentido, podemos comparar uma fórmula plana e uma condensada da molécula encontrada na gasolina. Basicamente, são fórmulas formadas por Carbono e Hidrogênio.
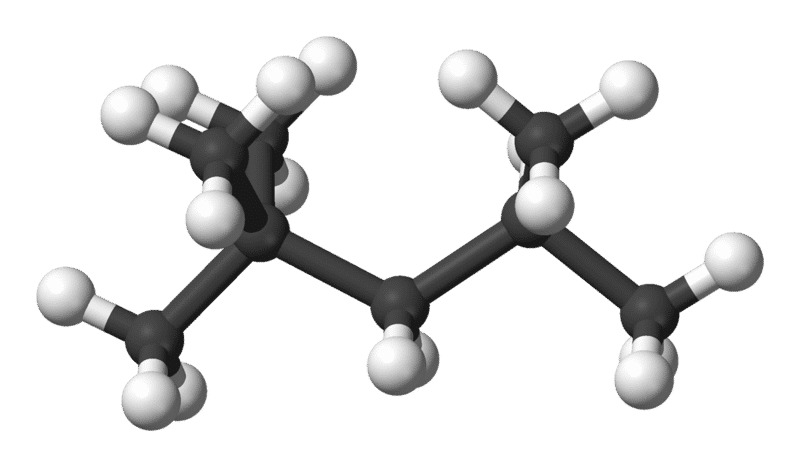
Portanto, na fórmula estrutural condensada, existe o número de átomos de oxigênio (2) e de Hidrogênio (3) explicando a fórmula de forma sintetizada.
Contudo, na fórmula estrutural plana, está explicitada a quantidade de átomos de hidrogênio (16) de carbono (10) e oxigênio (o), Por fim, na forma molecular, a quantidade de átomos está ao lado do símbolo do elemento, sendo a forma mais simplificada de representação de uma molécula.
Ligação covalente
Basicamente, as fórmulas químicas, entre elas, a fórmula estrutural, possuem uma única função, a de representar a união entre átomos. Portanto, esta ligação se dá por covalência, sendo denominada de ligação covalente.

Do mesmo modo, podemos concluir que a ligação covalente é o compartilhamento de elétrons entre átomos de um ou mais elementos que têm necessidade de receber elétrons. Neste sentido, os grupos de átomos unidos por ligação covalente são denominados moléculas.
A princípio, os elementos que tendem a fazer ligações covalentes são os não metais e os semimetais. Além disso, o número de ligações covalentes que o átomo de um elemento pode fazer, é chamado de valência desse elemento. Neste sentido, alguns elementos têm as seguintes características,
Exemplos:
- H e Cl ( hidrogênio e cloro) – monovalentes: podem fazer uma ligação
- O (oxigênio) – Bivalente: pode fazer duas ligações
- N (nitrogênio) – trivalente: pode fazer três ligações
- C ( carbono) – tetravalente: pode fazer quatro ligações.
Então, o que achou do texto sobre a fórmula estrutural? Se gostou, leia também: Condensação, o que é? Conceito, principais características e exemplos
Fontes: Brasil Escola, Toda Matéria, Manual de Química
Imagens: Quora, Revista Vidro Impresso e Sinapse