Na termodinâmica, o conceito de calor se refere à transição de energia, ou seja, temperatura entre um corpo e outro. Nesse sentido, há dois tipos de calor, o calor latente e o calor sensível.
No calor latente, a temperatura da substância é responsável pela mudança do estado físico da matéria, ou seja, quando a composição das moléculas sofre alguma alteração.
Já no calor sensível, o que ocorre é a apenas a mudança de temperatura, sem que a substância mude de estado físico.
Sendo assim, no caso do calor latente, é possível medir quanto uma substância precisa ceder ou receber de calor para que o estado físico seja alterado. Vale lembrar que, enquanto a mudança ocorre, a temperatura em si não se altera, então, a variação é desprezada.
Calor latente
O calor latente é uma grandeza física que determina qual a quantidade de calor que uma substância necessita para ceder ou receber energia térmica.
Neste caso, a energia faz com o que a grandeza física da matéria se altere, mas mantém constante a temperatura.
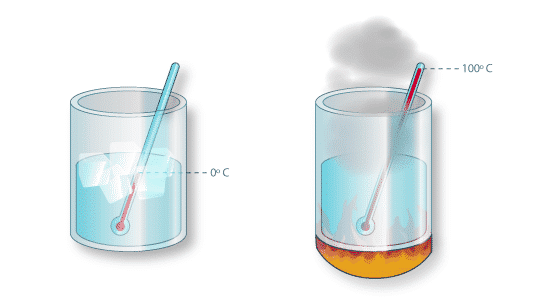
Todo o processo ocorre em um sistema termodinâmico, onde o estado físico se altera quando a matéria atinge temperatura de ebulição ou fusão, durante o momento de aquecimento.
A temperatura permanece a mesma, até a substância atingir o ponto de fusão ou ebulição – por conta da energia potencial que se acumula durante o aquecimento. Com isso, as moléculas que compõem a matéria permanecem agregadas, até que a energia suficiente seja absorvida ou cedida.
Quando ocorre a absorção necessária de energia, ou a energia térmica necessária é cedida, as moléculas da substância começam a se desagregar. Assim, a mudança de estado físico ocorre a partir do momento em que a interação diminui e as substâncias se alteram.
A unidade de medida utilizada para medir o calor latente é Joule por quilograma (J/kg), de acordo com o Sistema Internacional (SI).

Logo, nos cálculos, é analisada a quantidade de calor para que uma substância mude o estado físico. Além de J/kg, a unidade de caloria por grama também é comumente utilizada.
Um exemplo muito comum de calor latente é quando colocamos água para aquecer. Ou seja, a água só inicia o processo de evaporação quando a temperatura atinge 100ºC. O calor latente, então, é a energia térmica necessária para que ocorra o processo de mudança do estado físico.
Tipos de calor latente
Quando se fala em calor é possível dividi-lo de duas formas: calor latente e calor sensível. Como dito anteriormente, o calor latente é a energia necessária que uma substância cede ou absorve ao mudar de estado físico, mantendo a temperatura constante.
O que ocorre, então, é uma transferência de calor e, por isso, o calor latente também é conhecido como calor de transformação.

Já no calor sensível ocorre a transição de energia, porém não há mudança de estado físico, mas a temperatura se altera. Neste caso, a temperatura da substância se altera, mas o estado físico permanece o mesmo.
No caso do calor latente, podemos dividir as transformações em duas partes:
- Calor latente de fusão – como o próprio nome sugere, ocorre no momento do processo de fusão, ou seja, quando o calor é absorvido ou cedido na transformação do estado líquido para o sólido ou do sólido para o líquido. A temperatura, em ambos os casos, permanece constante.
- Calor latente de vaporização – ocorre no momento em que a substância passa do estado sólido para o líquido ou vice-versa, mantendo constante a temperatura.
Fórmulas
Para calcular o calor latente e o calor sensível, é necessário utilizar fórmulas específicas. No caso da energia térmica latente, o valor do cálculo pode ser positivo ou negativo, dependendo se a transformação está recebendo ou cedendo calor.

Neste caso, quando a substância cede energia térmica o valor é negativo e ocorre no que chamamos de processo exotérmico, comum na liquefação e solidificação.
Agora, se a substância recebe calor, o valor do cálculo é positivo e ocorre no processo endotérmico, nas transformações de vaporização e fusão.
Sendo assim, para calcular o calor latente utilizamos a fórmula: Q = m . L
Onde,
Q: quantidade de calor (cal ou J);
m: massa (g ou Kg);
L: calor latente (cal/g ou J/Kg).
Já para o cálculo do calor sensível, a fórmula utilizada é: Q = m . c . Δθ.
Onde,
Q: quantidade de calor sensível (cal ou J)
m: massa do corpo (g ou Kg)
c: calor específico da substância (cal/g°C ou J/Kg.°C)
Δθ: variação de temperatura (°C ou K)
O que achou da matéria? Se gostou, confira também qual a definição de Diagrama de Fases e o que é Hádron.
Fontes: Brasil Escola, Brasil Escola, Toda Matéria e Só Física
Imagens: Brasil Escola, Escola Kids, UOL, Todo Estudo e Medium



