A termodinâmica é um método da física para entender as transformações de energia por meio das quantidades de calor e as fases de trabalho durante esse processo. Em outras palavras, são leis criadas para compreensão das relações entre calor, energia e trabalho.
Nesse sentido, essa ciência foi desenvolvida por pesquisadores no período da Revolução Industrial para melhorar a eficiência das máquinas. Isto inclui os motores de carros e refrigeradores, além das máquinas térmicas utilizadas no minério e petróleo. Ao passo que, ao cozinhar percebemos as matérias reagindo em diferentes condições de temperatura.
Por isso, vamos aprender um pouco mais sobre a termodinâmica, sua leis e transformações de energia. Ademais, utilizamos ferramentas derivadas desse método diariamente, como na turbina de avião, usinas termoelétricas e trabalhos que envolvem mecânica.
O que é termodinâmica?
Como dito anteriormente, a termodinâmica se baseia na temperatura, que se define pelo grau de agitação da moléculas. Além disso, o calor que troca energia térmica entre o corpos. Por último, a energia que proporciona capacidade para um corpo realizar o trabalho.

Por conseguinte, o sistema termodinâmico pode se relacionar com mais de um corpo, como também pode ser dividido em aberto, fechado ou isolado.
- Aberto: quando a massa e a energia são transferidas entre o sistema e o meio externo;
- Fechado: Existe apenas transferência de energia ou calor;
- Isolado: Neste caso não há transferências ou trocas.
De modo geral, os gases ideais ou perfeitos são usados nos estudos da termodinâmica. Sendo assim, as colisões entre as partículas e as paredes dos recipientes são elásticas com duração mínima.
A partir disso, o gás ideal produz um comportamento no sistema fechado com as seguintes grandezas físicas: pressão, volume, e temperatura. Isto porque, são essas variáveis que definem o estado termodinâmico de um gás.
Em suma, o movimento das partículas do gás dentro do recipiente produz a pressão (p). No entanto, o volume (v) é formado pelo espaço ocupado do gás no interior do recipiente. Ao passo que, a energia cinética média das partículas do gás em movimento se refere a temperatura (t).
Por outro lado, a energia interna ajuda a medir como ocorrem as transformações pelas quais o gás passa. Portanto, se utilizarmos o gás ideal com apenas um tipo de átomo, teremos uma energia interna proporcional à temperatura. Isto se mede nesta fórmula: U = 3/2.n.R.T
Sendo que:
U= energia interna;
n= n° mols do gás;
R= constante universal dos gases ideais;
T= temperatura.
As quatros leis da termodinâmica
Primeiramente, existem quatros leis fundamentais que determinam a termodinâmica nos estudos da física. São elas: Lei Zero, Primeira Lei, Segunda Lei e Terceira Lei.
1- Lei Zero
Esta é uma lei da termodinâmica definida pelo equilíbrio térmico, visto que estabelece condições para manter os materiais em sintonia. Ao passo que, existem três pontos a serem observados:
- 1º: se um corpo A está em equilíbrio térmico em contato com um corpo B;
- 2º: e se esse corpo A está em equilíbrio térmico em contato com um corpo C;
- 3º: logo, B está em equilíbrio térmico em contato com C.
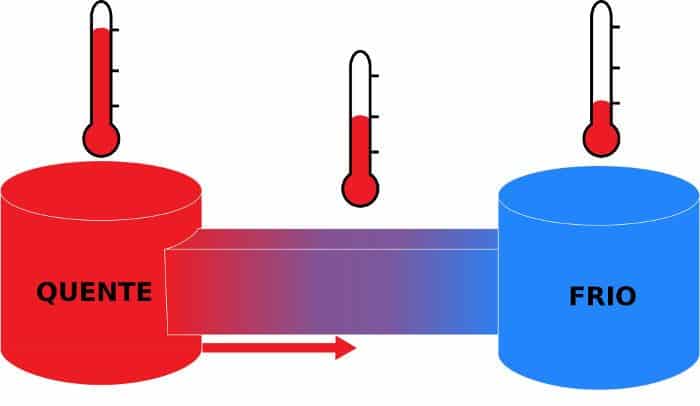
Nesse sentido, o corpo mais quente sempre deve transferir o calor para o mais frio. Isto porque, essa ação permite que as temperaturas se igualem, resultando no equilíbrio térmico.
Ademais, o nome de Lei Zero foi escolhido porque este entendimento se faz necessário antes da primeira e da segunda lei da termodinâmica.
2- Primeira lei
Antes de tudo, essa lei defende a conservação de energia no sistema. Em outras palavras, é mais vantajoso transformar a energia, do que criar ou destruir para obter calor.

Dessa forma, se utilizarmos uma bomba para encher um balão, a força exercida faz o pistão abaixar no interior do objeto, isto faz com que a energia se transforme em calor.
Portanto, a fórmula para esta lei é a seguinte: Q = t + △U
Q = quantidade de calor
t = trabalho
△U = variação de energia interna
3- Segunda lei
Neste caso, o corpo mais quente transfere calor para o corpo mais frio, mas nunca ao contrário. Portanto, esse processo é considerado irreversível, visto que não é possível converter calor integralmente em outra forma de energia.

4- Terceira lei
Esta lei tem como objetivo estabelecer um ponto de referência para determinar a entropia. Esta que é a base da Segunda lei da termodinâmica.

No entanto, a conclusão do físico Walther Nernst de que um objeto pode ser esfriado até zero absoluto, foi considerada por outros físicos como impossível. Além disso, esta lei se tornou polêmica, pois ainda é discutida pelos estudiosos como apenas uma regra.
Por fim, o que achou dessa matéria? Se gostou, confira também: Razão e proporção, o que são? Conceitos, propriedades e aplicações
Fontes: Descomplica, Toda Matéria e Brasil Escola
Imagens: BetaEQ, Barriquand, Mundo Educação, Quebra galho, Sooluciona e P&R



