O número atômico corresponde ao número de prótons existentes no núcleo dos átomos. Sendo que o número atômico é representado pela letra Z maiúscula.
Cada elemento químico tem o seu próprio número atômico. Sendo assim, não existem átomos de elementos químicos diferentes com o mesmo número atômico.
Em outras palavras, não existem elementos diferentes com a mesma quantidade de prótons.
Portanto, os números atômicos dos elementos torna mais fácil a classificação e a constituição da tabela periódica.
Enfim, de maneira geral, eles são representados na parte inferior do elemento, enquanto a massa (A) está na parte superior: zXA
Como determinar o número atômico de um elemento?
Em síntese, o número atômico é igual ao número de prótons no núcleo do átomo. Desse modo, para saber a quantidade de prótons de um átomo, é preciso determinar o valor de Z.
Por exemplo, o cálcio tem no seu núcleo 20 prótons e 20 nêutrons. Portanto, o número atômico do cálcio é 20.
Além disso, outra forma de determinar o número atômico de um elemento é conhecendo a quantidade de elétrons que ele possui.
Isso porque, os átomos são eletricamente neutros e têm a mesma quantidade de partículas com carga positiva e negativa, ou seja, de prótons e elétrons.
Dessa maneira, sabendo a quantidade de elétrons de um átomo neutro, podemos determinar a quantidade de prótons.
Por exemplo, o carbono tem 6 elétrons. Como o átomo é eletricamente neutro, o carbono deve ter em seu núcleo 6 prótons, já que tem 6 elétrons. Desse modo, o seu número atômico é 6.
Um detalhe importante é que os átomos podem receber ou perder elétrons de outros elementos químicos, formando íons positivos ou negativos.
Sendo assim, quando isso ocorre, o número de elétrons e de prótons no átomo não é mais igual.
Portanto, tenha cuidado ao determinar qual é o número atômico de um íon com base na quantidade de elétrons.
Como identificar o número atômico na Tabela Periódica?
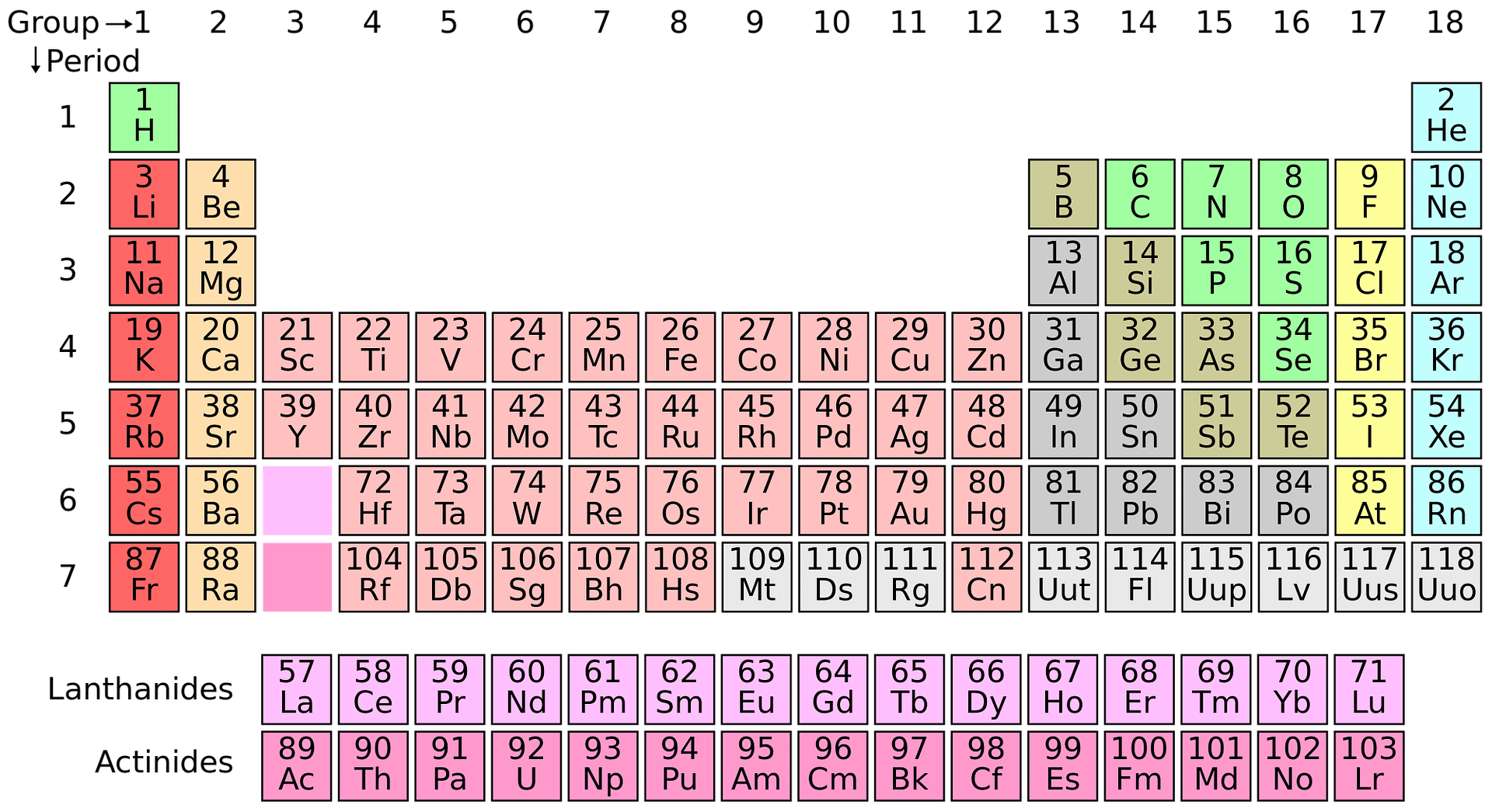
Em resumo, na Tabela Periódica, os elementos químicos são organizados no sentido crescente de número atômico, começando pelo hidrogênio (Z = 1) e indo até o oganessônio (Z = 118).
Sendo assim, é fácil identificar os números atômicos de cada elemento na Tabela Periódica. Isso porque, ele costuma aparecer do lado esquerdo do símbolo do elemento.
Enfim, observe na imagem abaixo como os elementos aparecem na tabela periódica e como as informações estão distribuídas:
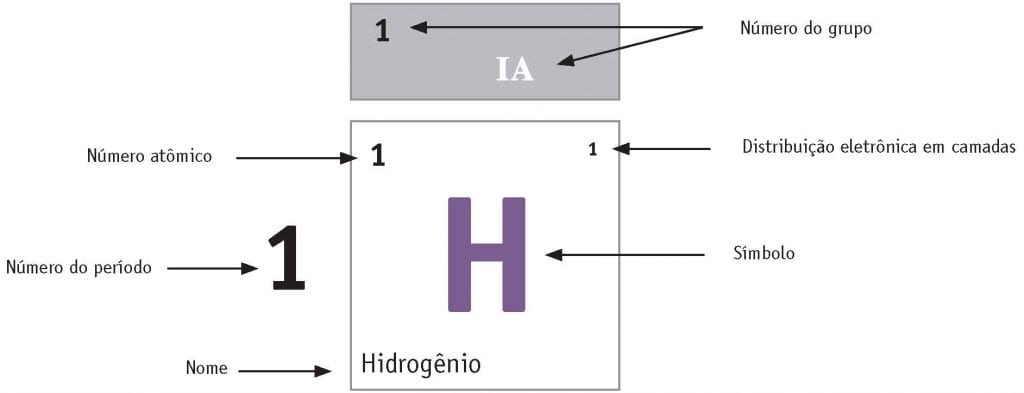
Qual a importância do número atômico?
Primeiramente, conhecer o número atômico é importante, pois ele é uma das características de um elemento químico.
Dessa forma, ele também é uma propriedade importante dos átomos e permiti a obtenção de outras informações sobre ele.
Sendo que essa propriedade define a posição de um elemento na Tabela Periódica. Inclusive, as propriedades periódicas variam de forma conhecida na tabela.
Desse modo, ao conhecer o número atômico de um elemento, é possível prever a sua posição, suas propriedades periódicas e principais características.
Além disso, o número atômico é importante para a determinação da quantidade de elétrons na eletrosfera, já que o número de elétrons e prótons é igual para átomos neutros.
Por fim, conhecer o número atômico é importante pois ele possibilita a determinação da distribuição eletrônica do átomo, característica importante para a determinação da natureza das ligações químicas.
Número atômico e Número de Massa
Como você já sabe, o número atômico (Z) corresponde ao número de prótons de um elemento químico. Por outro lado, o número de massa (A) representa a soma dos prótons mais os nêutrons.
Ou seja, configuram a estrutura de um elemento químico. Lembrando que os elementos químicos têm números atômicos diferentes.
Em resumo, para que o cálculo no número de massa seja realizado, é necessário utilizar uma fórmula específica. Neste caso, a fórmula é representada da seguinte forma: A = p + n.
Enfim, o número atômico (Z) se localiza na parte inferior, enquanto o número de massa está posto na parte superior.
Origem do número atômico
A Tabela Periódica foi proposta por Dmitri Mendeleev, em 1860. Sendo que ele se baseou em observações experimentais, mas tinha um respaldo teórico ainda frágil.
Posteriormente, Wilhelm Röntgen deu início a pesquisas com raios X, em 1896. Isso incentivou vários estudos sobre a interação desse tipo de radiação com a matéria.
Já em meados de 1903, Charles Grover Barkla investigou a interação entre os raios X e os elementos gasosos.
Em resumo, ele notou que a forma como a radiação era emitida se alterava de acordo com a posição que o elemento ocupava na Tabela Periódica.
Posteriormente, em 1913, o físico Henry Moseley ampliou o conhecimento de Barkla para outros elementos químicos.
Sendo que ele também reconheceu a forte correlação de regularidade entre os espectros de raios X e a posição do elemento na tabela.
Sendo assim, o físico chegou a propor que este comportamento estaria ligado ao número de elétrons de cada elemento.
Dessa maneira, Moseley atribuiu valores numéricos aos elementos químicos de acordo com as mudanças regulares registradas em seus espectros de raios X.
Com o passar do tempo, o físico conseguiu definir que o número atômico, na verdade, reflete o número de prótons de um átomo.
Portanto, essa foi uma descoberta muito importante. Isso porque, ela impactou as leis periódicas propostas por Mendeleev, onde eram explicadas inicialmente com base no número de massa.
Enfim, a descoberta do número atômico ocorreu durante experimentos de interação entre raios X e diversos elementos químicos.
Dessa forma, isso levou a uma explicação teórica para as propriedades químicas periódicas. Isso levando em conta a estrutura atômica dos átomos.
Sendo assim, a Tabela Periódica passou a ser ordenada em sentido crescente de números atômicos.
Exercícios
Por fim, resolva os exercícios abaixo para testar os seus conhecimentos sobre número atômico:
Unesp (2004)
Os “agentes de cor”, como o próprio nome sugere, são utilizados na indústria para a produção de cerâmicas e vidros coloridos. Tratam-se, em geral, de compostos de metais de transição, e a cor final depende, entre outros fatores, do estado de oxidação do metal, conforme mostram os exemplos na tabela a seguir.
| Coloração | Agente de cor | Estado de oxidação | Número atômico |
| Verde | Cr (crômio) | Cr3+ | 24 |
| Amarela | Cr (crômio) | Cr6+ | 24 |
| Marrom-amarelada | Fe (ferro) | Fe3+ | 26 |
| Verde-azulada | Fe (ferro) | Fe2+ | 26 |
| Azul-clara | Cu (cobre) | Cu2+ | 29 |
Com base nas informações fornecidas na tabela, é correto afirmar que:
a) o número de prótons do cátion Fe2+é igual a 24.
b) o número de elétrons do cátion Cu2+é 29.
c) Fe2+e Fe3+não se referem ao mesmo elemento químico.
d) o cátion Cr3+possui 21 elétrons.
e) no cátion Cr6+o número de elétrons é igual ao número de prótons.
Udesc
Na Inglaterra, por volta de 1900, uma série de experimentos realizados por cientistas, como Sir Joseph John Thompson (1856-1940) e Ernest Rutherford (1871-1937), estabeleceu um modelo do átomo que serviu de base à teoria atômica. Atualmente, sabe-se que três partículas subatômicas são os constituintes de todos os átomos: prótons, nêutrons e elétrons. Dessa forma, o átomo constituído por 17 prótons, 18 nêutrons e 17 elétrons possui número atômico e número de massa, sequencialmente, iguais a:
a) 17 e 18
b) 34 e 52
c) 17 e 17
d) 17 e 35
e) 35 e 17
Gabarito
Unesp (2004) O certo é a opção d)
Udesc A opção certa é d).
LEIA MAIS
Hibridização do carbono, aprenda tudo sobre o conteúdo
Quem foi Linus Pauling, o químico que ganhou 2 Prêmios Nobel
O que é Matéria? Propriedades gerais e específicas
Isomeria: aprenda o que é e quais são os tipos
Ligações químicas: tipos, funções e regras
Polaridade das moléculas – Eletronegatividade e geometria molecular
Fontes: Toda Matéria, Brasil Escola, Brasil Escola e, por fim, Khan Academy.