Basicamente, os elementos químicos presentes no primeiro grupo da tabela periódica são os Metais Alcalinos. Portanto, eles são chamados de família 1A, pois pertencem aos elementos que reagem facilmente com a água.
Assim, os metais alcalinos, formam as substâncias alcalinas, como os hidróxidos. A propósito, o sódio (Na) e o potássio (K), são os metais alcalinos mais abundantes no planeta.
A descoberta dos Metais Alcalinos foi feita gradativamente por vários cientistas e em épocas diferentes. O Lítio, por exemplo, foi descoberto em 1817, pelo sueco Johan August Arfwedson no mineral petita. Além disso, também é possível encontrar o lítio em outros minerais como: espodumênio, lepidolita, ambligonita e trifilita.
No entanto, alguns elementos foram preparados e outros descobertos. O sódio foi preparado pela primeira vez em 1807, por Humphry Davy, ao estudar a eletrólise ( passagem da corrente elétrica) de soluções alcalinas, principalmente as de soda cáustica.
Mas afinal, quais são as características dos Metais Alcalinos? Vamos descobrir agora!
Características dos Metais Alcalinos
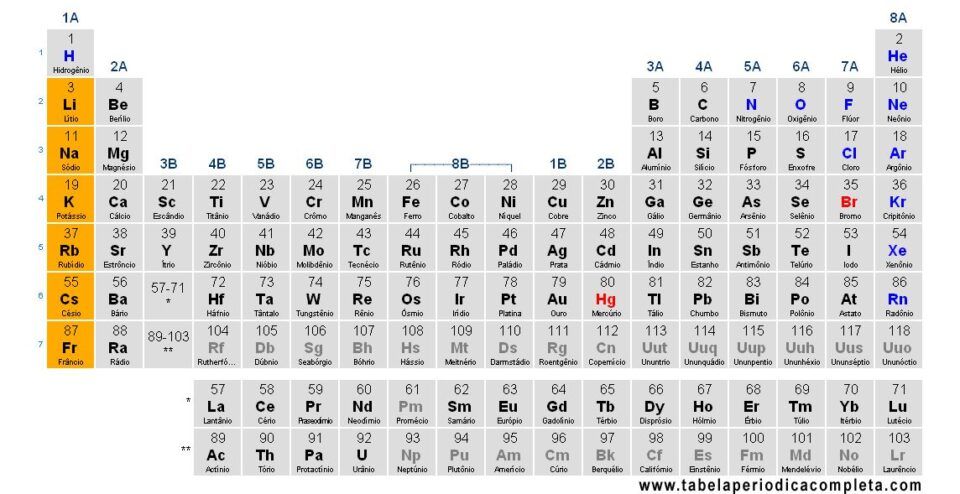
A família 1A da Tabela Periódica corresponde aos metais alcalinos que, no geral, é formada pelos seguintes elementos: Lítio (Li), Sódio (Na), Potássio (K), Rubídio (Rb), Césio (Cs) e Frâncio (Fr).
Basicamente, os elementos químicos que fazem parte desta família são sólidos em temperatura ambiente, possuem boa condução de eletricidade, com grande potencial reativo, bem como possuem baixa densidade. Além disso, também são características dos metais alcalinos:
- Característica mole e colorida;
- Potencial de ionização e baixa eletronegatividade;
- Alto nível de eletropositividade;
- Formam hidróxidos quando reagem com a água;
- Formam óxidos quando reagem com o oxigênio;
- Configuração eletrônica sempre terminando em n1.
Reações
Primeiramente, quando os metais alcalinos reagem com água, produzem H2 mais o correspondente hidróxido. Assim, a reação torna-se mais vigorosa à medida que descemos no grupo. Por exemplo:
- 2M H2O – 2M OH H2
- 2Li H2O – 2Li OH H2
- 2Na H2O – 2Na OH H2
- 2K H2O – 2KOH H2
Basicamente, nas reações com o ar atmosférico, os metais alcalinos se tornam quimicamente mais reativos, e perdem o brilho. Contudo, quando expostos ao ar seco, o sódio (Na), o potássio (K), e o Césio (Cs), por exemplo, formam óxidos de vários tipos.
Propriedades físico-químicas
Primeiramente, as propriedades dos metais alcalinos, referem-se a sua instabilidade e consequentemente a sua radioatividade. Portanto, podemos elencar algumas propriedades:

- Baixa eletronegatividade: esta propriedade é decrescente com o número de camadas, resultando no frâncio como menos eletronegativo;
- Baixa energia de ionização;
- Apenas os três últimos metais alcalinos são essencialmente radioativos.
Basicamente, podemos especificar estas propriedades a cada elemento do primeiro grupo da tabela:
- Lítio (Li): Basicamente, em relação ao grupo, é o mais duro, baixa solubilidade, menor densidade.
- Sódio (Na): Mole, baixa densidade, solubilidade moderada. Contudo, é altamente reativo e bom condutor de eletricidade. Assim, forma hidróxidos com a água e óxido com o oxigênio.
- Potássio (K): mole, baixa densidade, forte condutor de eletricidade. Portanto, é altamente reativo, e com boa solubilidade. Forma hidróxido com a água e óxido com o oxigênio.
- Rubídio (Rb): Mole, baixa densidade e grande solubilidade. Forma hidróxido e óxido.
- Césio (Cs): Mole, baixa densidade e alta solubilidade. Contudo, em suas reações com a água e o oxigênio, forma hidróxidos e óxidos
- Frâncio (Fr): Mole, baixa densidade e excelente solubilidade. Também forma hidróxidos e óxidos.
Nomenclatura dos Metais Alcalinos
De forma geral, vale lembrar que o nome “metal alcalino” significa que eles reagem facilmente com a água. Portanto, com essa reação, se forma hidróxido, substâncias básicas e alcalinas. Em síntese, essas substâncias são formadas pela liberação de hidrogênio. Além disso, eles reagem com o oxigênio, formando óxidos.

Basicamente, para exemplificar um hidróxido, lembramos da soda cáustica, utilizada na fabricação de papel, tecidos, detergentes. O hidróxido de sódio, ou soda cáustica, cuja fórmula é NaOH, é produzido por eletrólise.
O hidrogênio, que está no primeiro grupo da tabela periódica, é classificado como não-metal, porque a energia utilizada para retirar seu elétron é muito maior que a de qualquer outro elemento dessa família.
Gostou da matéria? Se gostou veja também, Tabela Periódica, O que é. Função, história, elementos, famílias
Fontes: Toda matéria, Manual da Química, Info Escola
Imagens: Tabela Periódca Completa, Manual da Química e Registro de Marca



