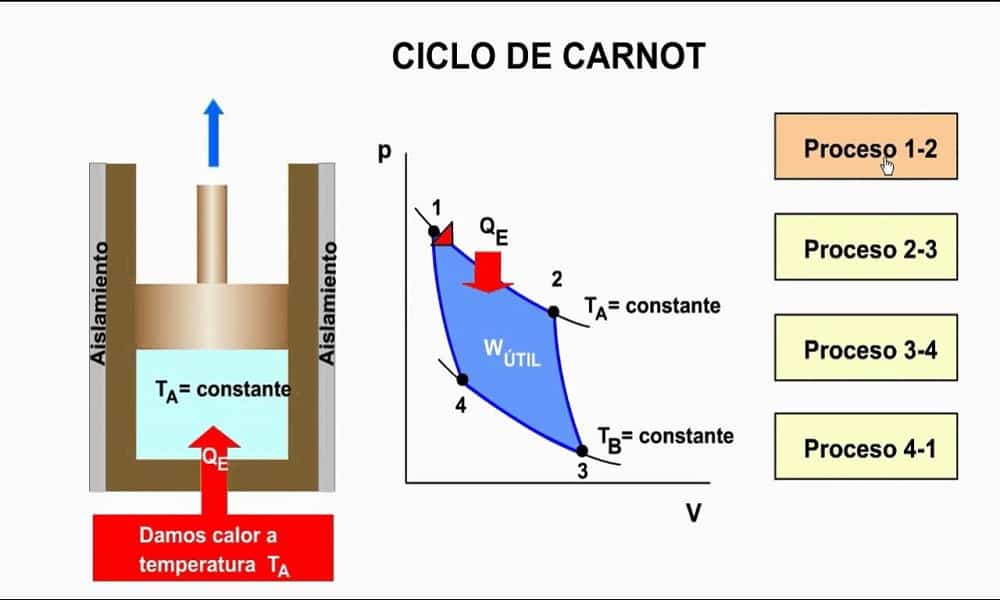
O Ciclo de Carnot é um ciclo particular que transforma termodinamicamente um gás ideal. Esse ciclo é executado pela máquina hipotética que foi criada pelo engenheiro Carnot.
Ela funciona entre duas transformações isotérmicas e duas adiabáticas que se alternam. Isso proporciona que se perca menos calor para o meio externo.
A Máquina de Carnot produz a quantia máxima que uma máquina térmica rende se trabalhar entre temperaturas da fonte quente e fria. Isso serve para orientar, por exemplo, a indústria sobre a viabilidade de se adquirir certo equipamento.
Contexto Histórico
Até o século XIX, supunha-se que seria viável construir uma máquina térmica capaz de transformar em trabalho toda a energia fornecida. Essa máquina ideal conseguiria, em tese, alcançar um rendimento total.
Foi então que o engenheiro francês Nicolas Carnot contestou tais assertivas e provou que isso não seria possível. Ele idealizou uma máquina térmica teórica capaz de chegar ao rendimento total, dentro de um ciclo de rendimento máximo. Isso ficou conhecido como Ciclo de Carnot. A tal máquina jamais poderia ser alcançada na realidade prática.
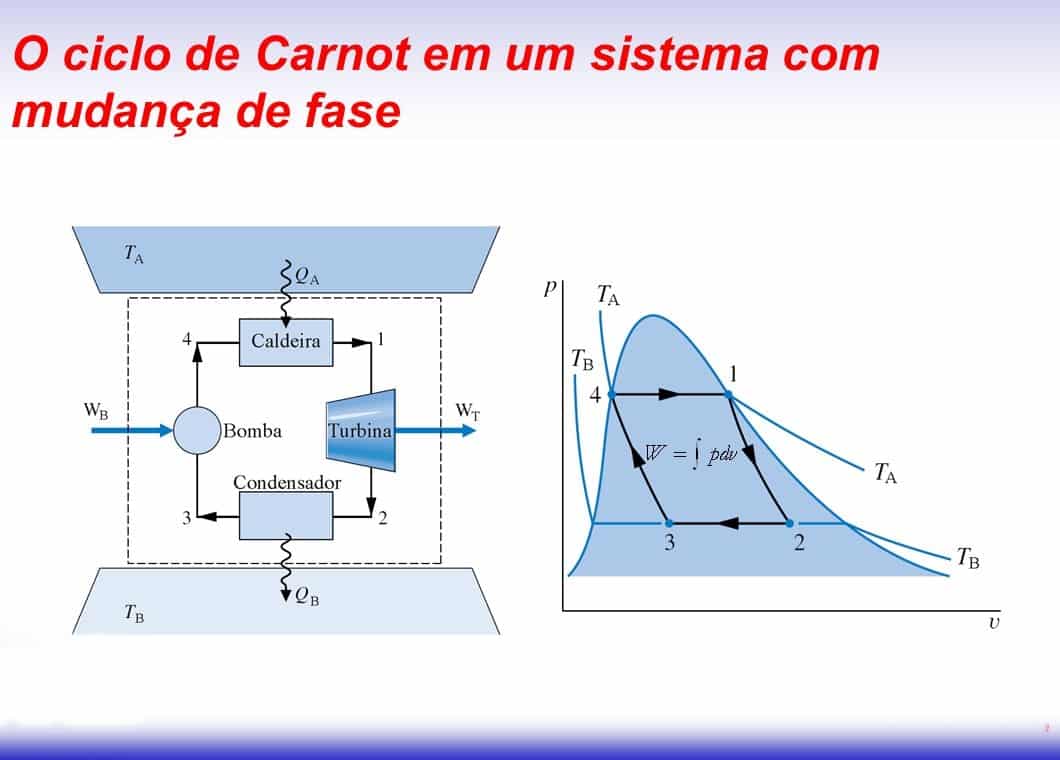
O Ciclo de Carnot se daria em quatro processos não importando a substância, a saber:
- Expansão isotérmica reversível: há o recebimento de calor da fonte de aquecimento (L-M);
- Expansão adiabática reversível: não há troca de calor com as fontes térmicas (M-N);
- Compressão isotérmica reversível: há a cessão de calor para a fonte de resfriamento (N-O);
- Compressão adiabática reversível: não há troca calor com as fontes térmicas (O-L).
Como funciona o Ciclo de Carnot
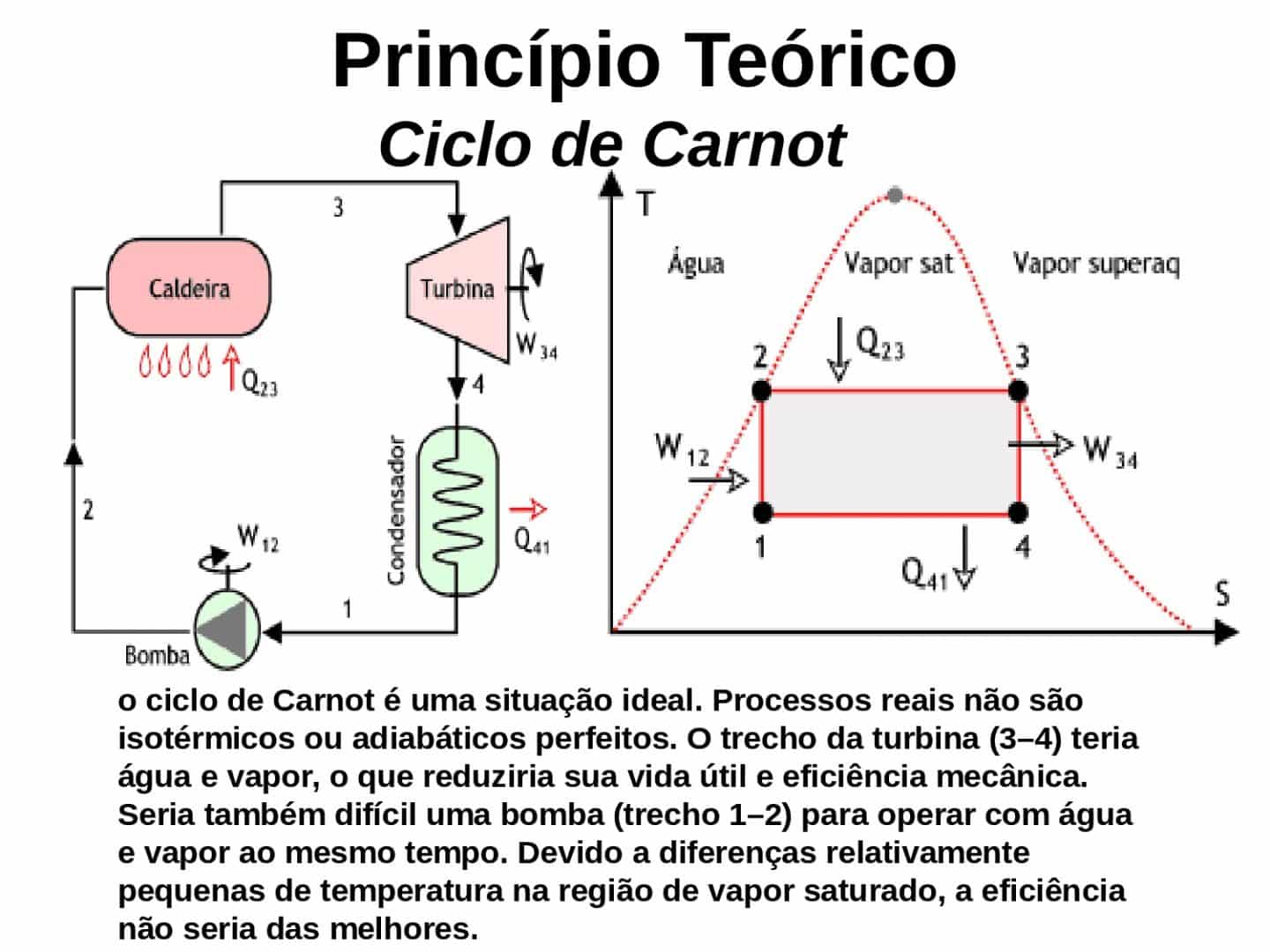
O Ciclo de Carnot começa a funcionar quando o gás sofre uma transformação isotérmica. Ele então expande e absorve uma quantia de calor “Q1”, que vem de uma fonte quente à temperatura “T1”.
Depois de passar pela transformação isotérmica, o gás sofrerá transformação adiabática, ou seja, sem trocas de calor com o meio. Expandindo de forma adiabática, sua temperatura despenca para um valor T2.
O gás então é compressado de forma isotérmica, liberando uma quantia de calor Q2 numa fonte fria à temperatura T2. Por fim, ele volta ao que era no início, posto que sofre uma compressão adiabática.
A utilidade da Máquina de Carnot
A Máquina de Carnot é uma idealização, embora ela não renda 100%. Só que representa a quantia máxima que uma máquina térmica pode render trabalhando entre temperaturas da fonte quente e fria.
Ela serve para se descobrir se uma máquina térmica rende bem, compensando o custo para um empreendimento. Não é possível qualquer máquina térmica render mais ou igual que a de Carnot, desde que opere entre duas fontes às temperaturas T1 e T2.
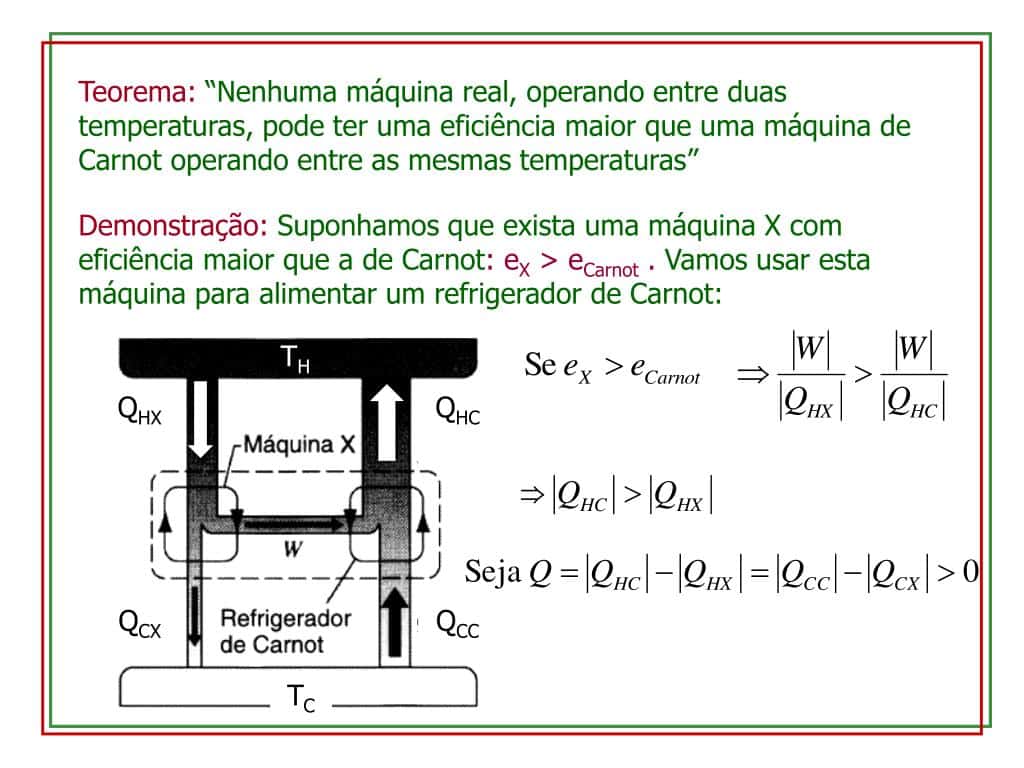
Só se sabe o quanto uma máquina térmica rende utilizando-se o cociente do trabalho pela energia útil. O trabalho é encontrado pela diferença entre a energia útil e a energia dissipada. Dessa forma, equação do rendimento é a diferença entre a unidade e o quociente da energia que se dissipou pela energia útil.
Podemos citar a antiga locomotiva a vapor como exemplo, posto que a caldeira é a fonte quente. Parte da energia térmica que dela provém é convertida em trabalho mecânico, já a outra parte é dissipada pelo ar.
O rendimento da Máquina de Carnot é apurado pelo cálculo da fórmula seguinte: R = 1 – T2/T1. Onde, “R” é o quanto rende a máquina de Carnot, “T1” é a temperatura em Kelvin (K) da origem quente e “T2” a temperatura da fonte fria em Kelvin (K).
Leia também sobre as Reações inorgânicas – o que são, como se classificam e exemplos.
Fonte: Wikipédia, Só Física, Info Escola, Mundo Educação, Toda Matéria, Alunos Online e Universo Racionalista.
Fonte das Imagens: Conhecimento Geral, Side Player, Docsite, Slide Serve.