O que você pensa ao ouvir o temo bateria? Algumas pessoas vão se lembrar dos dispositivos que dão vida à eletrônicos como celulares, computadores etc. Por outro lado, também podem imaginar aquele equipamento musical tocado por músicos em shows de rock.
As baterias usadas em celulares, e em tantos outros eletrônicos, são caracterizadas como um conjunto de pilhas ligadas em série. Ou seja, em termos químicos, as baterias são dispositivos eletroquímicos. Assim, para que possam funcionar, dependem de reações de oxidorredução que resultam em corrente elétrica.
Já a bateria utilizada por músicos em shows, por exemplo, é formada por vários instrumentos que são tocados de forma simultânea. Para se ter uma ideia, essa bateria formulada com o intuito de gerar som já era utilizada pelos antepassados. Porém, ganhou a forma como a conhecemos apenas no final do século 19.
Vamos conhecer um pouquinho sobre os dois tipos de bateria!
Definição de bateria
A primeira bateria da história foi construída por Alessandro Volta, em 1800, na Itália. O químico e físico é considerado o pioneiro da eletricidade. Isso porque, foi o criador da pilha voltaica, além de descobrir o primeiro método para a geração de eletricidade.
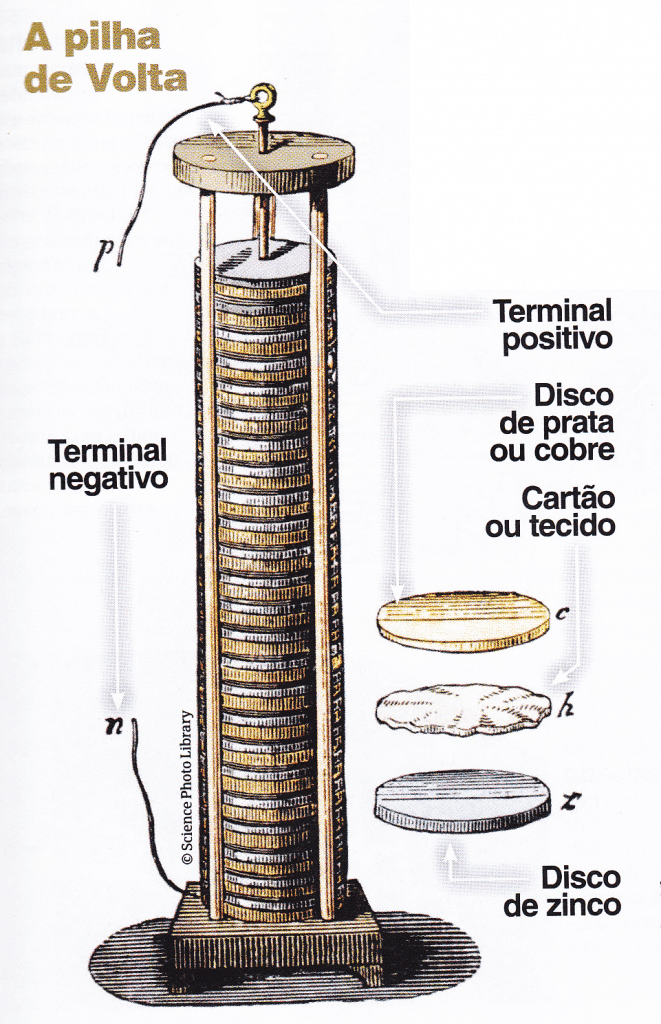
Como dispositivo químico, a bateria também pode ser chamada de pilha secundária, bateria secundária ou acumulador. Isso porque, são dispositivos que, assim que acaba a carga, podem ser recarregados. Neste caso, as pilhas primárias – pilhas comuns -, são aquelas que não podem ser recarregadas.
Nesse sentido, a formação de uma bateria consiste na presença de um ânodo (elétrodo carregado positivamente) e um cátodo (elétrodo com carga negativa). Assim, ambos os elétrodos ficam em contato com um condutor elétrico denominado de eletrólito.
Dessa forma, o conjunto de pilhas que formam uma bateria se ligam por conta da presença do polo positivo e o negativo dos elétrodos. Assim, as ligações podem ocorrer em série ou de forma paralela. Visto isso, uma das características que as baterias possuem é a de serem recarregadas quando a carga elétrica que produzem acaba.
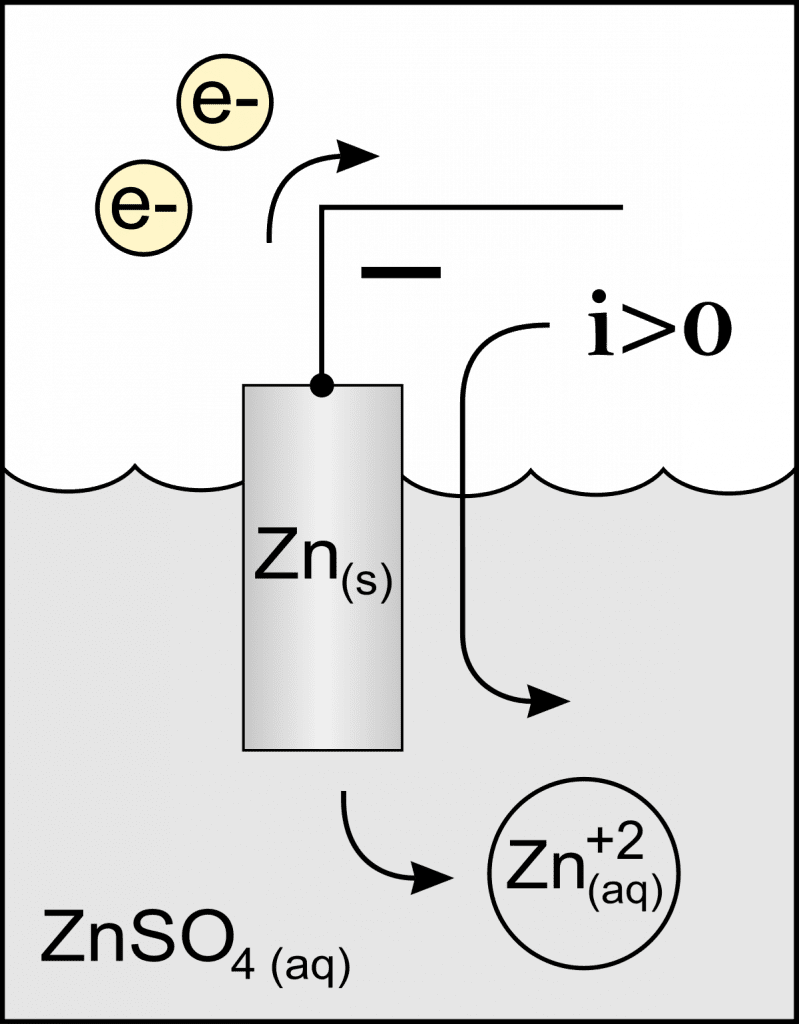
Neste caso, uma bateria fornece energia elétrica a partir das reações de oxidação e redução. Ou seja, quando ocorre a oxidação o elétrodo perde elétrons, já na redução o elétrodo ganha elétrons. Assim, quando a bateria para de funcionar significa que o elétrodo da oxidação acabou. Logo, com a recarga da bateria o elétrodo da oxidação é formado novamente.
Tipos de baterias
As baterias são classificadas de acordo com a finalidade. Visto isso, são utilizadas em diferentes situações dependendo da demanda. Além disso, apresentam diferentes elementos químicos nos elétrodos. Confira:
Bateria de chumbo/ácido
São as baterias caracterizadas pelas presença de metal de cumbo no ânodo e dióxido de cumbo (PbO2) no cátodo. Além disso, os elétrodos estão inseridos em uma solução aquosa com ácido sulfúrico (H2SO4).
Nesse sentido, a reação eletroquímica que ocorre faz com o que o metal chumbo sofra oxidação no ânodo. Por conta disso, o elétrodo perde elétrons. Em seguida, ocorre a interação com os ânions sulfato (SO4-2) resultando no sal sulfato de cumbo II: Pb + SO4-2 → PbSO4 + 2.
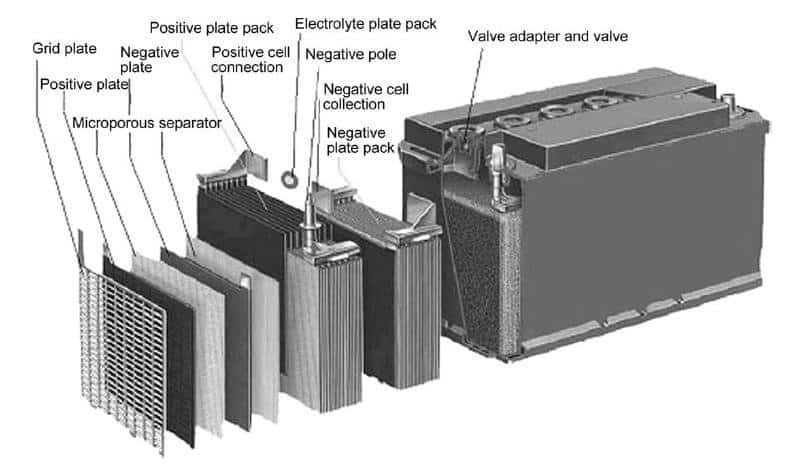
De maneira simultânea, o dióxido de chumbo presente no cátodo sofre redução. Em seguida, interage com os íons H+ e SO4-2 do ácido. A partir disso, forma-se água e sulfato de cumbo II: PbO2 + 4H+ + SO4-2 → PbSO4 + 2H2O + 2.
Visto isso, esse tipo de bateria é muito utilizado em veículos como:
- Carros de passeio
- Caminhões
- Motos
Bateria níquel/cádmio
São caracterizadas por possuir o ânodo formado por liga metálica de ferro e cádmio. Além disso, o cátodo apresenta na formação o hidróxido de níquel III (NiO(OH)2). Além disso, os elétrodos ficam imersos em solução aquosa, neste caso a água, além do hidróxido de potássio.
A partir disso, o cádmio sofre oxidação no ânodo. Por conta disso, ocorre a perda de elétrons na reação. Em seguida, há interação com os cátions hidróxido (OH–): Cd + OH– → Cd(OH)2 + 2.
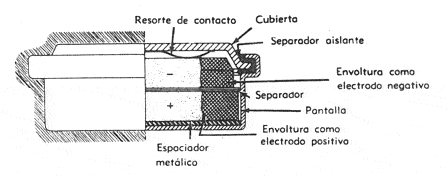
De forma paralela, ocorre redução no hidróxido de níquel III. Isso porque, o elemento entra em contato com a água presente na solução recebendo os elétrons que foram perdidos na primeira reação. Assim, o hidróxido de níquel III ganha os elétrons formando o hidróxido de níquel II hidratado. Por conta disso, ânions hidróxido são liberados: NiOOH + 2 H2O + 2e → Ni(OH)2.H2O + OH-.
Nesse sentido, esse tipo de bateria é utilizada em aparelhos como:
- Máquinas fotográficas
- Celulares
- Notebooks
- Filmadoras
- Telefones sem fio
- Brinquedos eletrônicos de uma forma geral.
Bateria hidreto metálico/óxido de níquel
A reação eletroquímica que ocorre na bateria hidreto metálico é semelhante ao que ocorre com a bateria níquel. Entretanto, o que diferente as duas reações é a utilização do hidreto metálico ao invés da liga de cádmio. Vale lembrar que o hidreto metálico é um elemento químico eletronegativo, sendo acompanhado por um metal das famílias IA ou IIA.
Visto isso, o processo de oxidação na bateria hidreto ocorre com o hidrogênio. Ou seja, ocorre a perda de elétron e, em seguida, ocorre a interação entre os íons OH–. Como resultado, água e um metal são formados. Já em relação ao cátodo, ocorre a mesma reação da bateria de níquel, ou seja, NiOOH + 2 H2O + 2e → Ni(OH)2.H2O + OH–.
Bateria de íons lítio
É caracterizada pela formação do ânodo e cátodo por meio da associação de lítio e grafite, além do óxido formado por lítio e cobalto respectivamente. Dessa forma, o carbono sofre oxidação no ânodo e, em seguida, libera os íons lítio e elétrons: LiyC(s) → C(s) + yLi+.

De forma simultânea, no cátodo ocorre a chegada dos elétrons junto dos íons lítio. Em seguida, os íons se incorporam ao óxido que foi formado por lítio e cobalto na reação anterior. Por conta disso, ocorre o aumento da quantidade de lítio no óxido: LiCoO(s) + Li+ + e → Li2CoO(s).
Bateria na ciência
As baterias, como já vimos, são dispositivos que precisam ser recarregados. Entretanto, cientistas da Universidade da Califórnia, em Irvine, criaram uma bateria que dura a vida toda. E acreditem, a descoberta ocorreu por acidente. Isso porque, os cientistas estavam testando formas de substituir o o lítio líquido das baterias por opções mais seguras.
Em uma das tentativas, descobriram que na utilização de nanocabos de ouro recobertos com um gel de eletrólitos as baterias se tornavam 400 vezes mais eficientes e resistentes que as baterias convencionais. Dessa forma, a bateria conseguiria realizar até 200 mil ciclos de carga sem a necessidade de ser recarregada. Contado que, uma bateria comum morre após 7 mil ciclos de energia, no máximo.

Os nanocabos de ouro proporcionaram esse resistência devido a estrutura fina – milhares de vezes mais fino que o cabelo humano. Além disso, são estruturas que conduzem eletricidade com estrema facilidade e possuem uma superfície em que os elétrons ficam armazenados. Dessa forma, os elétrons conseguem ser transferidos de forma mais fácil.
Isso significa que, se as baterias de Irvine fossem utilizadas em aparelhos eletrônicos, por exemplo, teriam vida mais longa que as baterias convencionais. Entretanto, como são feitas com nanocabos de ouro, a produção em grande massa seria algo muito caro. Assim, os cientistas estudam a possibilidade de substituir o ouro por algum metal comum, como no caso do níquel.
Bateria na música
A bateria, instrumento essencial em bandas, ganhou forma no final do século 19. A partir disso, criou-se um instrumento que reunia diversos outros instrumentos tocados simultaneamente. Porém, nossos antepassados já utilizavam recursos parecidos com o da bateria para produzir sons em rituais sagrados.

Assim, os “homens das cavernas”, desenvolviam instrumentos feitos com troncos de árvores e revestidos com pele de animais. Visto isso, os primeiros instrumentos de percussão foram encontrados em escavações na região da Morávia, na República Tcheca. Dessa forma, a bateria foi se modernizando e ganhando novas funções com o passar dos anos.
Com isso, os pratos de metal – um dos instrumentos que compõem a bateria – surgiram na Assíria (atual território de Israel), durante o século 12 a.C. O equipamento era utilizado para substituir os tambores de maneira e produziam um som bem diferente.
Evolução
Já no século 14 a bateria ganha novos materiais que eram utilizados para compor a estrutura dos tambores. Além disso, o som produzido pelos batuques passam a ser mais altos, chamando mais atenção. Por conta disso, eram utilizados em desfiles militares. No século 17, é a fez das orquestras utilizarem do instrumento nas apresentações.

Enquanto isso, na década de 1890, o pedal foi inventado e os tambores que eram tocados por pessoas diferentes passam a ser manuseados por um percussionista. Assim, o músico conseguia tocar todos os tambores de forma simultânea. Dessa forma, em 1930, surgem as primeiras baterias com chimbal, caixa e bumbo. Por fim, em 1990 surgem as baterias eletrônicas. Com a evolução, pequenas esferas imitam os sons dos pratos e tambores, além de reproduzirem outros tipos de som.
Você sabia?
- Em 2019 os cientistas John B. Goodenough, M. Stanley Whittingham e Akira Yoshino ganharam o prêmio Nobel de Química pela criação da bateria de íon de lítio.
O que achou da matéria? Se gostou, corre pra conferir como ocorre a Corrosão dos Metais e o que é Hidrólise.
Fontes: Super Abril, BBC, Portal São Francisco e Manual da Química
Fonte imagem destaque: Oficina da Net



