O éter é um tipo de função orgânica oxigenada. Isso porque, ele tem um átomo de oxigênio entre duas cadeias carbônicas, que são formadas por átomos de carbono e hidrogênio.
Ou seja, ele é um composto orgânico que pertence à função oxigenada, já que tem oxigênio em sua composição. Desse modo, ele é formado por dois radicais orgânicos (carbono) ligados a um átomo de oxigênio.
Sendo que, quando ele tem mais de quatro carbonos por oxigênio, o éter se torna solúvel em água. Além disso, ele é, em geral, pouco reativo.
O éter pode ficar em estado sólido, líquido ou gasoso.
Enfim, ele é um composto muito inflamável, que tem um cheiro forte e intenso. Inclusive, a sua inalação pode causar dependência.
Vale destacar que éster não é a mesma coisa que éter. Isso porque, o éter tem função solvente, ao passo em que o éster é flavorizante.
Características e propriedades
Primeiramente, o éter é caracterizado por apresentar geometria angular, portanto, o éter é polar.
O seu ponto de fusão, quando comparado ao de outros compostos orgânicos de massa molar aproximada, se assemelha ao dos alcanos, apesar de ser menor do que os de outros compostos orgânicos.
Além disso, em temperatura ambiente, quando possui quatro ou mais átomos de carbono ele se apresenta em estado físico de liquidez.
Entretanto, se comparados com a água, apresenta uma densidade pequena.
O éter interage por meio de interações de hidrogênio. Isso porque, eles apresentam baixa polaridade, o que os leva a interagir entre si por meio de uma fraca interação dipolo permanente.
Ele é caracterizado ainda por exalar um odor forte e agradável, mas cuja inalação pode provocar dependência. Por fim, o éter pode ser classificado como simétrico ou assimétrico.
-
O simétrico é ligado ao oxigênio por dois radicais idênticos.
-
O assimétrico é ligado ao oxigênio por dois radicais diferentes.
Nomenclatura oficial do éter
A nomenclatura oficial do éter é feita da seguinte forma:
Prefixo do radical menor + óxi + prefixo do radical maior + infixo + o
Em resumo, para fazer a nomenclatura oficial de um éter, é essencial definir qual é o seu ligante maior e qual é o seu ligante menor.
Para você entender melhor como isso é feito, vamos a um exemplo da aplicação dessa regra de nomenclatura:
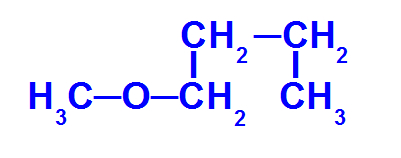
Acima temos os seguintes radicais:
-
Metil (CH3-)
-
Butil (CH3-CH2-CH2-CH2-)
Sendo assim, para fazer a nomeação deste composto, temos:
prefixo do radical menor: Met
+
oxi
+
prefixo do radical maior: but
+
an (pois ele apresenta apena ligações simples)
+
o
Portanto, o nome deste éter é metóxibutano.
Nomenclatura usual do éter
A nomenclatura usual é feita da seguinte forma:
Éter + nome dos radicais (mais simples e, depois, o mais complexo) + ico
ou
Nomes dos radicais + éter
Para você entender como isso funciona na prática, vamos para um exemplo. Observe o composto abaixo:
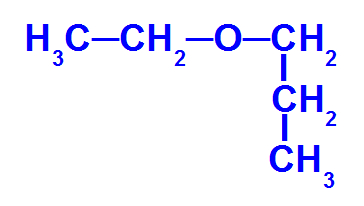
Neste composto, temos os seguintes radicais:
-
Etil (CH3-CH2-)
-
Propil (CH3-CH2-CH2-)
Sendo assim, para fazer a nomeação temos:
Éter
+
radical menor: etil
+
prefixo do radical maior: propil
+
ico
Portanto, o seu nome é éter etil-propílico, ou também pode ser etil-propil-éter.
Para que servem?
O éter é muito útil como solvente. Desse modo, ele é muito utilizado em laboratórios para remoção de gorduras.
Além disso, ele é usado fora do ambiente laboratorial, em oficinas mecânicas, por exemplo, para remover graxa e tintas.
Ele é útil ainda na extração de essências, como de flores, madeira, etc.
Enfim, uma curiosidade é que, antigamente, o éter também servia como anestésico em cirurgias e procedimentos médicos.
No entanto, como ele é um composto inflamável e tóxico, deixou de ser usado por questões de segurança.
Diferença entre éteres e ésteres
Apesar dos nomes parecidos, os éteres e os ésteres são diferentes. Os dois são funções orgânicas oxigenadas, mas a cadeia dos éteres é mais simples.
Isso porque, ele é composto por oxigênio entre duas cadeias de carbono.
Além disso, os ésteres são formados por oxigênio entre duas cadeias de carbono e hidrogênio ligado à hidroxila e carbonilo entre carbonos.
Enfim, existe ainda a diferença de que os éteres são muito usados como solventes, já os ésteres são substâncias flavorizantes.
Fontes: Brasil Escola, Info Escola, e, por fim, Toda Matéria.



