Todo mundo conhece uma pilha, mas será que todo mundo sabe, realmente, o que são esses dispositivos? Por isso hoje vamos aprender sobre as pilhas, a sua definição, funcionamento e principais componentes.
Primeiramente que as pilhas, ou células galvânicas para ser mais científico, são dispositivos que transforam energia química em energia elétrica por meio de um processo espontâneo. Em outras palavras, as pilhas fornecem energia ao sistema até que uma reação química termine.
Sendo assim, e como as pilhas são muito usadas no cotidiano, hoje vamos falar sobre elas. Confira.
O que são Pilhas?
As pilhas são basicamente dispositivos que produzem corrente elétrica a partir de reações químicas. No caso, estamos falando propriamente da oxidação e da redução de componentes metálicos que compõem sua estrutura. Portanto, vamos explicar o que é cada uma dessas reações a seguir:
- Oxidação: é a capacidade que um material apresenta de perder elétrons;
- Redução: é a capacidade que um material apresenta de ganhar elétrons.
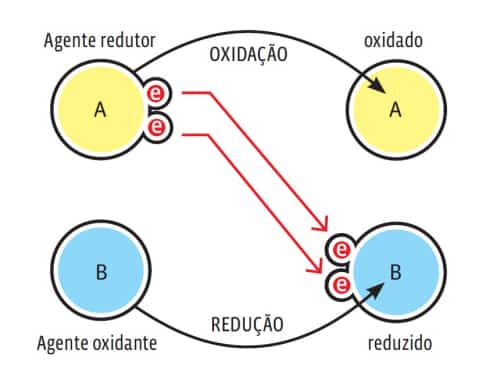
Sendo assim, em uma pilha, os elétrons saem de um componente e chegam até outro, formando assim uma corrente elétrica. Essa que por sua vez é capaz de fazer funcionar diversos dispositivos eletrônicos, como controles e etc.
A primeira pilha criada foi inventada por Alessandro Volta, no ano de 1800. Na época, o dispositivo, ainda primitivo, era formado por discos de zinco e cobre separados por um algodão embebido em salmoura. Assim, o tal conjunto de discos era colocado de forma intercalado, um em cima do outro, formando um empilhado de discos. Por isso o nome, porque formava uma pilha de discos.
Funcionamento das Pilhas
Contudo, para explicar como funciona uma pilha, iremos usar o modelo de uma das primeiras pilhas já feitas, a pilha de Daniell. Confira abaixo:
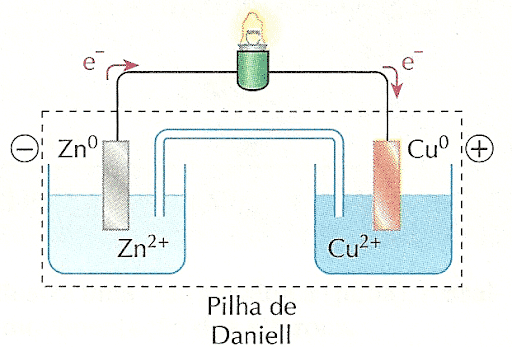
Na pilha de Daniell, temos:
- Um ânodo de zinco (formado por uma placa) imerso em uma solução formada por água e sulfato de zinco (ZnSO4). A placa de zinco, ao sofrer oxidação, libera elétrons, formando o cátion Zn+2, que permanece na solução. Com isso, a placa tem seu tamanho diminuído e a solução fica com excesso de cátions;
- Um cátodo de cobre (formado por uma placa) imerso em uma solução formada por água e sulfato de cobre (CuSO4). Na solução, existem cátions cobre (Cu+2), os quais, ao receber os elétrons vindos do ânodo, transformam-se em cobre sólido (Cu) e aderem-se à placa. Com isso, a placa tem seu tamanho aumentado e a solução fica com deficiência de cátions;
- Uma ponte salina, formada por uma solução de água e cloreto de potássio (KCl), que possui cátions potássio (K+) e ânions cloreto (Cl–). Sendo assim, durante o funcionamento da pilha, cátions da ponte salina deslocam-se para a solução do cátodo, e os ânions da ponte salina deslocam-se para a solução do ânodo;
- E por fim, um fio condutor conecta o ânodo ao cátodo.
As pilhas atuais seguem esse mesmo princípio de funcionamento, no qual um metal doa elétrons para outro, através de ma solução condutora, e assim produz a corrente elétrica.
No entanto, a diferença aqui é que as pilhas usadas hoje são secas. Isso porque não utilizam como eletrólito uma solução líquida, como acontece no exemplo demonstrado acima.
Componentes de uma Pilha
Todas as pilhas são formadas essencialmente por dois eletrodos, além de um eletrólito. Portanto temos:
- Ânodo: eletrodo negativo no qual acontece a reação de oxidação, ou seja, perda de elétrons;
- Cátodo: eletrodo positivo no qual acontece a reação de redução, ou seja, ganho de elétron;
- Solução eletrolítica (ponte salina): é o meio pelo qual os elétrons cedidos pelo ânodo chegam até o cátodo.
Exemplos de Pilhas
Atualmente existem uma enorme variedades de pilhas disponíveis no mercado. Contudo, as mais comuns são as pilhas ácidas (de Leclanché) e as pilhas alcalinas.
Mas além dessas, outros exemplos são as pilhas de lítio e iodo e as pilhas de mercúrio e zinco. Então, vamos conhecer melhor cada uma delas a seguir:
Pilha Ácida (pilha de Leclanché)
Essa foi a primeira pilha desenvolvida sem a necessidade de soluções líquidas. Estamos falando de uma pilha capaz de produzir uma voltagem em torno de 1,5 V.
Então as pilhas ácidas são compostas por:
- Um ânodo formado por zinco metálico;
- Um cátodo formado por uma pasta com cloreto de amônio, água, amido e dióxido de manganês;
- Uma ponte salina que serve como condutora para os elétrons que partem do cátodo em direção ao ânodo.
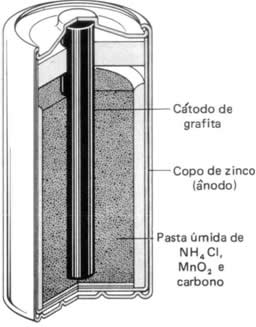
Essa é um exemplo de pilha muito usada em brinquedos e dispositivos eletrônicos gerais (controle remoto, lanternas etc.).
Pilha Alcalina
A pilha alcalina também apresenta o mesmo padrão de estrutura da pilha comum. Contudo, que a diferencia das pilhas comuns é a composição do ânodo e do cátodo. Essa pilha é capaz de produzir uma voltagem de 1,5 V.
Desse modo, esses são os seus componentes:
- Um ânodo formado por zinco metálico ou cádmio;
- Um cátodo formado por óxido de mercúrio, óxido de níquel e iodo;
- Apresenta no material que compõe o cátodo uma base misturada.
Pilha de Lítio e Iodo
Já a pilha de lítio e iodo é mais potente do que as demais, isso porque é capaz de produzir uma voltagem em torno de 2,8 V.
Portanto, apresenta os seguintes componentes:
- Um ânodo formado por uma placa de lítio;
- Um cátodo formado por um complexo de iodo.
O exemplo mais comum da utilização desse tipo de pilha é em aparelhos de marca-passo.

Pilha de Mercúrio e Zinco
Por fim, a pilha de mercúrio e zinco, que produz uma voltagem em torno de 1,35 V.
Os seus componentes são:
- Um ânodo formado por uma placa de zinco;
- Um cátodo formado por uma pasta com óxido de mercúrio (HgO).
Esse tipo de pilha é comumente usado em relógios e calculadoras, entre outros dispositivos.

Então, agora que você aprendeu tudo sobre pilhas, que tal aprender como fazer fogo usando uma pilha?
Fontes: Manual da Química, Brasil Escola, Alunos Online
Fonte Imagem Destaque: VG Resíduos



