Os elementos químicos são agrupamentos de átomos, que têm a mesma quantia de prótons. Ou seja, tem o mesmo número atômico.
No total, existem 118 elementos químicos. Desse total, 92 são naturais, isto é, estão presentes na natureza. Já os 26 restantes são artificiais.
Esses elementos são representados na tabela periódica. Sendo que a tabela se divide em períodos e famílias. Além disso, os elementos podem ter propriedades periódicas ou aperiódicas.
Representação dos elementos químicos
Todos os elementos de que se tem conhecimento, estão na tabela periódica. Sendo que eles são representados por uma sigla.
Na sigla, a primeira letra é maiúscula. Se a sigla tiver mais de uma letra, a segunda será minúscula. Por exemplo, o elemento ferro é representado pela sigla Fe.
Além da sigla, na tabela estão alguns dados importantes sobre os elementos. Tais como: nome, símbolo, número atômico e massa atômica, por exemplo.
Classificação periódica dos elementos químicas
Os elementos estão presentes na tabela periódica por ordem crescente em relação ao número atômico. Sendo assim, eles são agrupados em períodos e famílias.
1- Períodos
Em resumo, os períodos são as sete linhas horizontais da tabela periódica. Sendo que os elementos têm o mesmo número de camadas eletrônicas. São eles:
-
1º Período: 2 elementos
-
2º Período: 8 elementos
-
3º Período: 8 elementos
-
4º Período: 18 elementos
-
5º Período: 18 elementos
-
6º Período: 32 elementos
-
7º Período: 32 elementos
2- Famílias
Por outro lado, os grupos, famílias ou colunas, são as 18 linhas verticais da tabela periódica. Dessa forma, as famílias A e B têm 8 grupos cada uma:
-
Família 1A; Metais Alcalinos (lítio, sódio, potássio, rubídio, césio e frâncio).
-
2A; Metais Alcalinos -Terrosos (berílio, magnésio, cálcio, estrôncio, bário e rádio).
-
3A; Família do Boro (boro, alumínio, gálio, índio, tálio e ununtrio).
-
4A; Família do Carbono (carbono, silício, germânio, estanho, chumbo e fleróvio).
-
5A; Família do Nitrogênio (nitrogênio, fósforo, arsênio, antimônio, bismuto e ununpêntio).
-
6A; Calcogênios (oxigênio, enxofre, selênio, telúrio, polônio, livermório).
-
7A; Halogênios (flúor, cloro, bromo, iodo, astato e ununséptio).
-
8A; Gases Nobres (hélio, neônio, argônio, criptônio, xenônio, radônio e ununóctio).
Além disso, os elementos de transição (metais de transição) são as 8 famílias da série B:
-
Família 1B; cobre, prata, ouro e roentgênio.
-
2B; zinco, cádmio, mercúrio e copernício.
-
3B; escândio, ítrio e sério de lantanídios (15 elementos) e actinídeos (15 elementos).
-
4B; titânio, zircônio, háfnio e rutherfórdio.
-
5B; vanádio, nióbio, tântalo e dúbnio.
-
6B; cromo, molibdênio, tungstênio e seabórgio.
-
7B; manganês, tecnécio, rênio e bóhrio.
-
8B; ferro, rutênio, ósmio, hássio, cobalto, ródio, irídio, meitnério, níquel, paládio, platina, darmstádio.
Quais são as propriedades dos elementos químicos?
Os elementos têm dois tipos de propriedades:
1- Propriedades periódicas
Esse tipo varia de forma periódica de acordo com o aumento ou redução dos números atômicos. São elas:
-
Raio Atômico
-
Volume Atômico
-
Densidade Absoluta
-
Ponto de Fusão e Ponto de Ebulição
-
Afinidade Eletrônica
-
Energia de Ionização
-
Eletronegatividade
-
Eletropositividade
2- Propriedades aperiódicas
Por outro lado, as aperiódicas são aquelas que não variam periodicamente. Exemplos disso são:
-
Massa Atômica
-
Calor Específico
Quais são os elementos químicos?
Confira abaixo a tabela com todos os elementos, seus símbolos, números atômicos e massas atômicas. Sendo que as massas atômicas entre parênteses são os isótopos mais estáveis dos elementos radioativos.
| Elemento | Símbolo | Número Atômico | Massa Atômica |
|---|---|---|---|
| Actínio | Ac | 89 | (227) |
| Alumínio | Al | 13 | 26,9815 |
| Amerício | Am | 95 | (243) |
| Antimônio | Sb | 51 | 121,75 |
| Argônio | Ar | 18 | 39,948 |
| Arsênio | As | 33 | 74,9216 |
| Astato | At | 85 | (210) |
| Bário | Ba | 56 | 137,34 |
| Berquélio | Bk | 97 | (247) |
| Berílio | Be | 4 | 9,0122 |
| Bismuto | Bi | 83 | 209 |
| Bóhrio | Bh | 107 | (262,1) |
| Boro | B | 5 | 10,811 |
| Bromo | Br | 35 | 79,909 |
| Cádmio | Cd | 48 | 112,40 |
| Cálcio | Ca | 20 | 40,08 |
| Califórnio | Cf | 98 | (251) |
| Carbono | C | 6 | 12,01115 |
| Cério | Ce | 58 | 140,12 |
| Césio | Cs | 55 | 132,905 |
| Chumbo | Pb | 82 | 207,19 |
| Cloro | Cl | 17 | 35,453 |
| Cobalto | Co | 27 | 58,93 |
| Cobre | Cu | 29 | 63,55 |
| Copernício | Cn | 112 | 285 |
| Criptônio | Kr | 36 | 83,80 |
| Cromo | Cr | 24 | 51,996 |
| Cúrio | Cm | 96 | (247) |
| Darmstádio | Ds | 110 | (269) |
| Disprósio | Dy | 66 | 162,50 |
| Dúbnio | Db | 105 | (262) |
| Einstênio | Es | 99 | (252) |
| Enxofre | S | 16 | 32,064 |
| Érbio | Er | 68 | 167,26 |
| Escândio | Sc | 21 | 44,956 |
| Estanho | Sn | 50 | 118,69 |
| Estrôncio | Sr | 38 | 87,62 |
| Európio | Eu | 63 | 151,96 |
| Férmio | Fm | 100 | (257) |
| Ferro | Fe | 26 | 55,847 |
| Fleróvio | Fl | 114 | 289 |
| Flúor | F | 9 | 18,9984 |
| Fósforo | P | 15 | 30,9738 |
| Frâncio | Fr | 87 | (223) |
| Gadolínio | Gd | 64 | 157,25 |
| Gálio | Ga | 31 | 69,72 |
| Germânio | Ge | 32 | 72,59 |
| Háfnio | Hf | 72 | 178,49 |
| Hássio | Hs | 108 | (265) |
| Hélio | He | 2 | 4,0026 |
| Hidrogênio | H | 1 | 1,00797 |
| Hólmio | Ho | 67 | 164,930 |
| Índio | In | 49 | 114,82 |
| Iodo | I | 53 | 126,9044 |
| Irídio | Ir | 77 | 192,2 |
| Itérbio | Yb | 70 | 173,04 |
| Ítrio | Y | 39 | 88,905 |
| Lantânio | La | 57 | 138,91 |
| Laurêncio | Lr | 103 | (260) |
| Lítio | Li | 3 | 6,941 |
| Livermório | Lv | 116 | 292 |
| Lutécio | Lu | 71 | 174,97 |
| Magnésio | Mg | 12 | 24,312 |
| Meitnério | Mt | 109 | (269) |
| Manganês | Mn | 25 | 54,9380 |
| Mendelévio | Md | 101 | (258) |
| Mercúrio | Hg | 80 | 200,59 |
| Molibdênio | Mo | 42 | 95,94 |
| Moscóvio | Mc | 115 | 288 |
| Neodímio | Nd | 60 | 144,24 |
| Neônio | Ne | 10 | 20,183 |
| Netúnio | Np | 93 | (237) |
| Nihônio | Nh | 113 | 284 |
| Nióbio | Nb | 41 | 92,906 |
| Níquel | Ni | 28 | 58,69 |
| Nitrogênio | N | 7 | 14,0067 |
| Nobélio | No | 102 | (259) |
| Oganessônio | Og | 118 | 294 |
| Ósmio | Os | 76 | 190,2 |
| Ouro | Au | 79 | 196,967 |
| Oxigênio | O | 8 | 15,9994 |
| Paládio | Pd | 46 | 106,4 |
| Platina | Pt | 78 | 195,09 |
| Plutônio | Pu | 94 | (244) |
| Polônio | Po | 84 | (209) |
| Potássio | K | 19 | 39,098 |
| Praseodímio | Pr | 59 | 140,907 |
| Prata | Ag | 47 | 107,870 |
| Promécio | Pm | 61 | (145) |
| Protactínio | Pa | 91 | (231) |
| Rádio | Ra | 88 | (226) |
| Radônio | Rn | 86 | (222) |
| Rênio | Re | 75 | 186,2 |
| Ródio | Rh | 45 | 102,905 |
| Roentgênio | Rg | 111 | (272) |
| Rubídio | Rb | 37 | 85,47 |
| Rutênio | Ru | 44 | 101,07 |
| Rutherfórdio | Rf | 104 | (261 |
| Samário | Sm | 62 | 150,35 |
| Seabórgio | Sg | 106 | (263,1) |
| Selênio | Se | 34 | 78,96 |
| Silício | Si | 14 | 28,086 |
| Sódio | Na | 11 | 22,9898 |
| Tálio | Tl | 81 | 204,37 |
| Tantálio | Ta | 73 | 180,948 |
| Tecnécio | Tc | 43 | (98) |
| Telúrio | Te | 52 | 127,60 |
| Tenessino | Ts | 117 | 294 |
| Térbio | Tb | 65 | 158,924 |
| Titânio | Ti | 22 | 47,90 |
| Tório | Th | 90 | 232,0 |
| Túlio | Tm | 69 | 168,934 |
| Tungstênio | W | 74 | 183,85 |
| Urânio | U | 92 | 238 |
| Vanádio | V | 23 | 50,942 |
| Xenônio | Xe | 54 | 131,38 |
| Zinco | Zn | 30 | 65,38 |
| Zircônio | Zr | 40 | 91,22 |
Exercícios resolvidos sobre os elementos químicos
Para colocar seus conhecimento em prática, tente resolver os exercícios abaixo:
Enem 2017
No ar que respiramos existem os chamados “gases Inertes”. Trazem curiosos nomes gregos, que significam “o Novo”, “o Oculto”, “o Inativo”. E de fato são de tal modo inertes, tão satisfeitos em sua condição, que não interferem em nenhuma reação química, não se combinam com nenhum outro elemento e justamente por esse motivo ficaram sem ser observados durante séculos: só em 1962 um químico, depois de longos e engenhosos esforços, conseguiu forçar “o Estrangeiro” (o xenônio) a combinar-se fugazmente com o flúor ávido e vivaz, e a façanha pareceu tão extraordinária que lhe foi conferido o Prêmio Nobel.
Qual propriedade do flúor justifica sua escolha como reagente para o processo mencionado?
- Densidade.
- Condutância.
- Eletronegatividade.
- Estabilidade nuclear.
- Temperatura de ebulição.
Enem 2018
Na mitologia grega, Nóbia era a filha de Tântalo, dois personagens conhecidos pelo sofrimento. O elemento químico de número atômico (Z) igual a 41 tem propriedades químicas e físicas tão parecidas com as do elemento de número atômico 73 que chegaram a ser confundidos. Por isso, em homenagem a esses dois personagens da mitologia grega, foi conferido a esses elementos os nomes de nióbio (Z = 41) e tântalo (Z = 73). Esses dois elementos químicos adquiriram grande importância econômica na metalurgia, na produção de supercondutores e em outras aplicações na indústria de ponta, exatamente pelas propriedades químicas e físicas comuns aos dois.
KEAN, S. A colher que desaparece: e outras histórias reais de loucura, amor e morte a partir dos elementos químicos. Rio de Janeiro: Zahar, 2011 (adaptado).
A importância econômica e tecnológica desses elementos, pela similaridade de suas propriedades químicas e físicas, deve-se a
- Terem elétrons no subnível f.
- Serem elementos de transição interna.
- Pertencerem ao mesmo grupo na tabela periódica.
- Terem seus elétrons mais externos dos níveis 4 e 5, respectivamente.
- Estarem localizados na família dos alcalinos terrosos e alcalinos, respectivamente.
UFG
O número de prótons, nêutrons e elétrons representados por 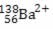
a) 56, 82 e 56
b) 56, 82 e 54
c) 56, 82 e 58
d) 82, 138 e 56
e) 82, 194 e 56
Gabarito
-
Enem 2017; o certo é a resposta C.
-
Enem 2018; o certo é a resposta C.
-
UFG; o certo é a alternativa B.
Fontes: Brasil Escola; Mundo Educação; Manual da Química; Brasil escola; Projeto agatha edu e, por fim; Toda Matéria.



