As aminas são compostos orgânicos, constituídos de uma cadeia carbônica ligada a um átomo de nitrogênio. Sendo assim, esses compostos são derivados da amônia (NH3), lugar onde ocorre à substituição de um, dois ou três átomos de hidrogênios por radicais orgânicos (R). Eles podem ser formados por grupos alquilas ou arilas.
Sendo assim, as aminas são classificadas de acordo com a quantidade de hidrogênios substituídos nesse processo. Portanto, são classificadas em três tipos, sendo elas:
- Amina primária: é formada pela substituição de um único hidrogênio da amônia por um radical orgânico (R-NH2);
- Amina secundária: é formada pela substituição de dois hidrogênios da amônia por dois radicais orgânicos (R1R2NH);
- Amina terciária: é formada pela substituição dos três hidrogênios da amônia por três radicais orgânicos (R1R2R3N).
Então, hoje vamos falar um pouco mais sobre essas substâncias orgânicas, as aminas. Confira.
Nomenclatura das Aminas
Primeiramente, vamos entender como acontece a nomenclatura dessas substâncias, seguindo as regras da IUPAC. Sendo assim, é importante ressaltar as diferenças entre os tipos de aminas existentes.
Começando pelas animas primárias, que senguem o esquema abaixo:
Prefixo + Infixo + Sufixo
Sendo o prefixo referente à quantidade de carbonos. Já o infixo referente ao tipo de ligação, podendo ser simples “an”, dupla “en” ou tripla “in”. E por fim o sufixo, que é a palavra amina.
Para o entendimento ficar mais fácil, observe os exemplos abaixo:
CH3 – CH2 – NH2
Nesse exemplo, note que há dois átomos de carbono, sendo assim, o prefixo será “et”. Quanto as ligações entre os átomos de carbono, elas são simples, então, o infixo fica “an”, e o sufixo amina. Nesse caso, o nome da substância é etanamina.
Fonte: InfoEscola
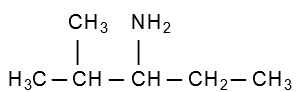
Contudo, se tiver insaturações ou ramificações na cadeia, como no exemplo acima, é necessário deixar claro na sua nomenclatura as posições na cadeia.
Desse modo, repare que a cadeia principal tem 5 carbonos, sendo assim o perfixo será “pent”. A ramificação no segundo carbono da cadeia, um grupo metil, assim a cadeia é insaturada, portanto o infixo será “an”. Já no carbono 3 está localizado o grupo amina. Sendo assim, o nome será 2-metil-pentan-3-amina.
Nomenclatura usual das Aminas
No entanto, quanto a nomenclatura mais comum das aminas, alguns autores usam uma sequência mais simplificada. Sendo ela: nome do radical ou radicais mais amina.
Contudo, no caso de houver radicais diferentes, deve-se seguir a ordem alfabética.
Confira os exemplos abaixo:
- Exemplo 1: Amina primária
H3C – CH2 – CH2 – NH2
Como na amina primária desse exemplo, há a presença de uma radical propil, o seu nome será propilamina.
- Exemplo 2: Amina secundária
H3C – NH – CH2 – CH3
Já nessa amina secundária, tem a presença do radical metil e do radical etil. Portanto, o seu nome é etil-metilamina, conforme a ordem alfabética,
- Exemplo 3: Amina Terciária
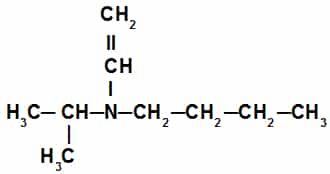
Por fim, a amina terciária, que tem a presença do radical isopropil, do radical butil e do radical vinil. Sendo assim, o seu nome é butil-isopropil-vinilamina.
Características das Aminas
Características Físicas das Aminas
No entanto, as aminas podem ser encontradas em três estados de agregação, sendo eles:
- Gases: aminas com 1 a 3 substituintes metil e a etilamina;
- Líquidas: da propilamina à dodecilamina;
- Sólidas: aminas com mais de 12 átomos de carbono.
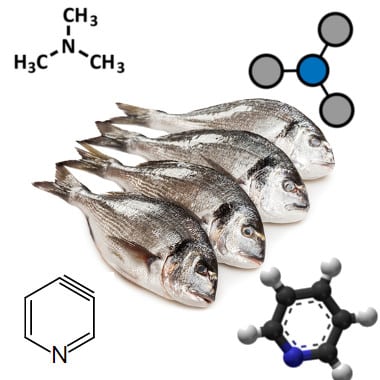
Contudo, tanto a metilamina quanto a etilamina possuem um cheiro semelhante ao da amônia. Sendo assim, as demais, tem um cheiro de peixe, esse que pode ser eliminado com o suco do limão. Aliás, uma das substâncias que dão o cheiro do peixo é a trimetilamina.
Portanto, as aminas aromáticas podem ser tóxicas e letais.
Características Químicas das Aminas
As aminas por sua vez são tidas como bases orgânicas, graças ao par eletrônico encontrado no átomo de nitrogênio presente nesses compostos.
Mais do que isso, essas substâncias também apresentam caráter básico, ou seja, na presenta de um ácido, elas provaram uma reação de neutralização.
Sendo assim, quanto maior for o caráter básico desse composto, maior será a chance de uma reação com outra substância.
Aplicações das Aminas
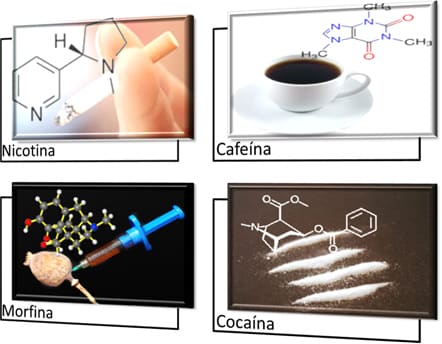
Por fim, a sua aplicação. No dia a dia, as aminas são encontradas em moléculas de várias substâncias estimulantes e em drogas. Entre elas, a cafeína, a nicotina, anfetaminas, cocaína e crack.
Contudo, as vitaminas fundamentais para a vida são também aminas, por isso o nome: “vital + amina”. Porém, nem todas as vitaminas são desse grupo funcional.
Além disso, também existem aminoácidos tanto nos alimentos quanto no nosso organismo. Esses que são formados com o grupo amino e pelo grupo carboxila.
Por fim, as animas aromáticas que também são muito comuns, sendo usadas na fabricação de corantes, tais como a anilina, e também de explosivos.
Sendo assim, agora que você já aprendeu o que são as aminas, que tal aprender também sobre Anidridos?
Fontes: Brasil Escola, InfoEscola, Manual da Química
Fonte Imagem Destaque: Etec



